正在加载图片...
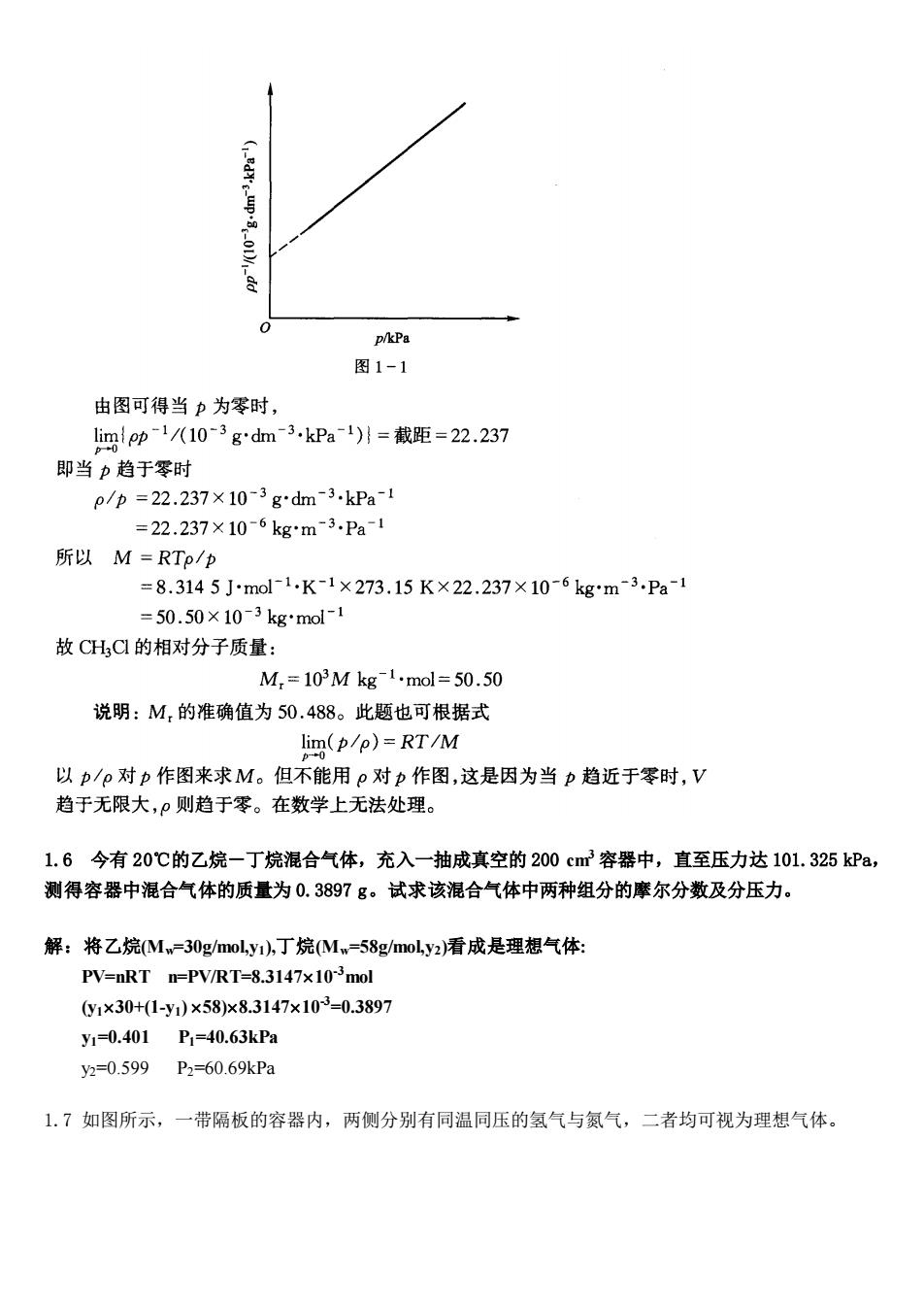
p/kPa 图1-1 由图可得当力为零时, limip-1/10-3gdm3.kPal)1=截距=22.237 即当力趋于零时 p/p=22.237×10-3gdm3.kPa-l =22.237×106kg*m3.Pa1 所以M=RTp/p =8.3145J小mol1.K-1×273.15K×22.237×10-6kgm3.Pa-1 =50.50×10-3 kg'mol-11 故CHC的相对分子质量: M,=103Mkg1mol=50.50 说明:M,的准确值为50.488。此题也可根据式 lim(p/p)=RT/M 以p/P对p作图来求M。但不能用p对p作图,这是因为当p趋近于零时,V 趋于无限大,则趋于零。在数学上无法处理。 1.6今有20℃的乙烷-丁烷混合气体,充入一抽成真空的200cm容器中,直至压力达101.325kPa, 测得容器中混合气体的质量为0.3897g。试求该混合气体中两种组分的摩尔分数及分压力。 解:将乙烷Mw=30 g/moL.y1).丁烷(Mw=58 z/moL.y2)看成是理想气体: PV=nRT n=PV/RT=8.3147x103mol y1×30+1-y1)×58)x8.3147×103=0.3897 y1=0.401 P1=40.63kPa y2=0.599P2=60.69kPa 1.7如图所示,一带隔板的容器内,两侧分别有同温同压的氢气与氮气,二者均可视为理想气体。1.6 今有 20℃的乙烷-丁烷混合气体,充入一抽成真空的 200 cm3 容器中,直至压力达 101.325 kPa, 测得容器中混合气体的质量为 0.3897 g。试求该混合气体中两种组分的摩尔分数及分压力。 解:将乙烷(Mw=30g/mol,y1),丁烷(Mw=58g/mol,y2)看成是理想气体: PV=nRT n=PV/RT=8.314710 -3mol (y130+(1-y1) 58)8.314710 -3 =0.3897 y1=0.401 P1=40.63kPa y2=0.599 P2=60.69kPa 1.7 如图所示,一带隔板的容器内,两侧分别有同温同压的氢气与氮气,二者均可视为理想气体