正在加载图片...
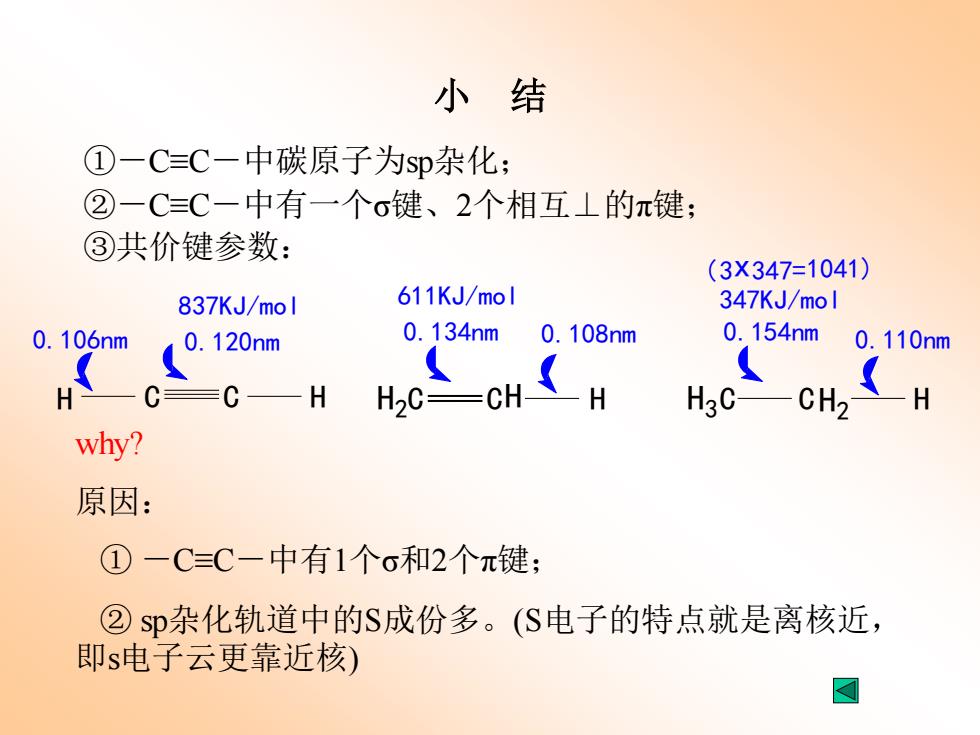
小结 ①一C=C一中碳原子为$p杂化; ②一C=C一中有一个σ键、2个相互⊥的π键: ③共价键参数: (3X347=1041) 837KJ/mol 611KJ/mol 347KJ/mol 0.106nm 0.120nm 0.134nm 0.108nm 0.154nm 0.110nm C=C—H H2C=CHH H3C— CH2 一H why? 原因: ①一C=C一中有1个σ和2个元键; ②sp杂化轨道中的S成份多。(S电子的特点就是离核近, 即s电子云更靠近核) 国 小 结 ①-C≡C-中碳原子为sp杂化; ②-C≡C-中有一个σ键、2个相互⊥的π键; ③共价键参数: 837KJ/mol 347KJ/mol ( ) H C C H 0.106nm 0.120nm 0.154nm 0.110nm H C C H 3 H2 3x347=1041 611KJ/mol 0.134nm 0.108nm H C CH H 2 why? 原因: ① -C≡C-中有1个σ和2个π键; ② sp杂化轨道中的S成份多。(S电子的特点就是离核近, 即s电子云更靠近核)