正在加载图片...
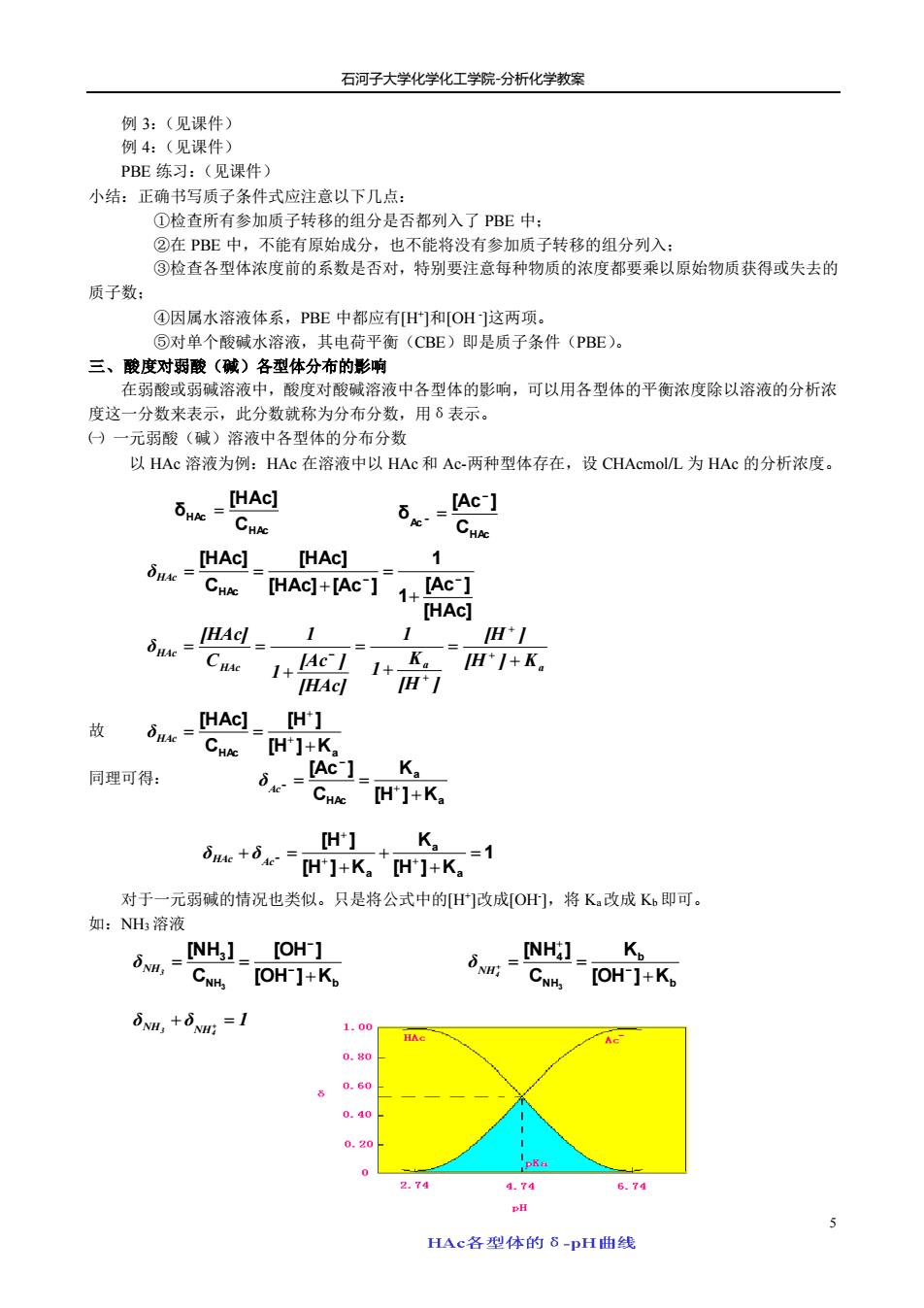
石河子大学化学化工学院分析化学教案 例3:(见课件) 例4:(见课件) PBE练习:(见课件) 小结:正确书写质子条件式应注意以下几点: ①检查所有参加质子转移的组分是否都列入了PBE中: ②在PBE中,不能有原始成分,也不能将没有参加质子转移的组分列入: ③检查各型体浓度前的系数是否对,特别要注意每种物质的浓度都要乘以原始物质获得或失去的 质子数: ④因属水溶液体系,PBE中都应有旧]和[OH这两项。 ⑤对单个酸碱水溶液,其电荷平衡(CBE)即是质子条件(PBE)。 三、酸度对弱酸(碱)各型体分布的影响 在弱酸或弱碱溶液中,酸度对酸碱溶液中各型体的影响,可以用各型体的平衡浓度除以溶液的分析浓 度这一分数来表示,此分数就称为分布分数,用8表示。 ()一元弱酸(碱)溶液中各型体的分布分数 以HAc溶液为例:HAc在溶液中以HAc和Ac两种型体存在,设CHAcmol/L为HAc的分析浓度。 bd [Ac-] L[HAC_HAc】 1 Cwe [HAc]+Ac】1+Ac-】 [HAc] 1 5nw-Cue 1 AeL H*1 1+ H*I+K。 故 dk=HAq.【H】 CHe [H']+K 同理可得: _[Ac-]_K, -]+K. H】 K。 iae+ie“H]+K+H们K,1 对于一元弱碱的情况也类似。只是将公式中的日们改成[O],将K.改成K。即可。 如:NH溶液 30,=INH] [OH CNH [OH ]+Kp CNH.[OH-]+K SNM,+6Nm:=1 1,00 0.80 0.40 0.20 2.74 4.74 6.74 DH HAc各型休的8-pH曲线 石河子大学化学化工学院-分析化学教案 5 例 3:(见课件) 例 4:(见课件) PBE 练习:(见课件) 小结:正确书写质子条件式应注意以下几点: ①检查所有参加质子转移的组分是否都列入了 PBE 中; ②在 PBE 中,不能有原始成分,也不能将没有参加质子转移的组分列入; ③检查各型体浓度前的系数是否对,特别要注意每种物质的浓度都要乘以原始物质获得或失去的 质子数; ④因属水溶液体系,PBE 中都应有[H+ ]和[OH - ]这两项。 ⑤对单个酸碱水溶液,其电荷平衡(CBE)即是质子条件(PBE)。 三、酸度对弱酸(碱)各型体分布的影响 在弱酸或弱碱溶液中,酸度对酸碱溶液中各型体的影响,可以用各型体的平衡浓度除以溶液的分析浓 度这一分数来表示,此分数就称为分布分数,用δ表示。 ㈠ 一元弱酸(碱)溶液中各型体的分布分数 以 HAc 溶液为例:HAc 在溶液中以 HAc 和 Ac-两种型体存在,设 CHAcmol/L 为 HAc 的分析浓度。 故 同理可得: 对于一元弱碱的情况也类似。只是将公式中的[H+ ]改成[OH- ],将 Ka改成 Kb 即可。 如:NH3 溶液 HAc HAc C [HAc] δ = HAc Ac C [Ac ] δ − − = [HAc] [Ac ] 1 1 [HAc] [Ac ] [HAc] C [HAc] HAc − − + = + δHAc = = HAc a a HAc [H ] K [H ] [H ] K 1 1 [HAc] [Ac ] 1 1 C [HAc] δ + = + = + = = + + + − HAc Ka [H ] [H ] C [HAc] + = = + + δHAc a a HAc [H ] K K C [Ac ] + = = + − − Ac δ 1 [H ] K K [H ] K [H ] a a a = + + + + = + + + − HAc Ac δ δ NH b 3 [OH ] K [OH ] C [NH ] 3 + = = − − NH3 δ b b NH 4 [OH ] K K C [NH ] 3 + = = − + + NH4 δ δ δ 1 4 NH3 NH + + =