正在加载图片...
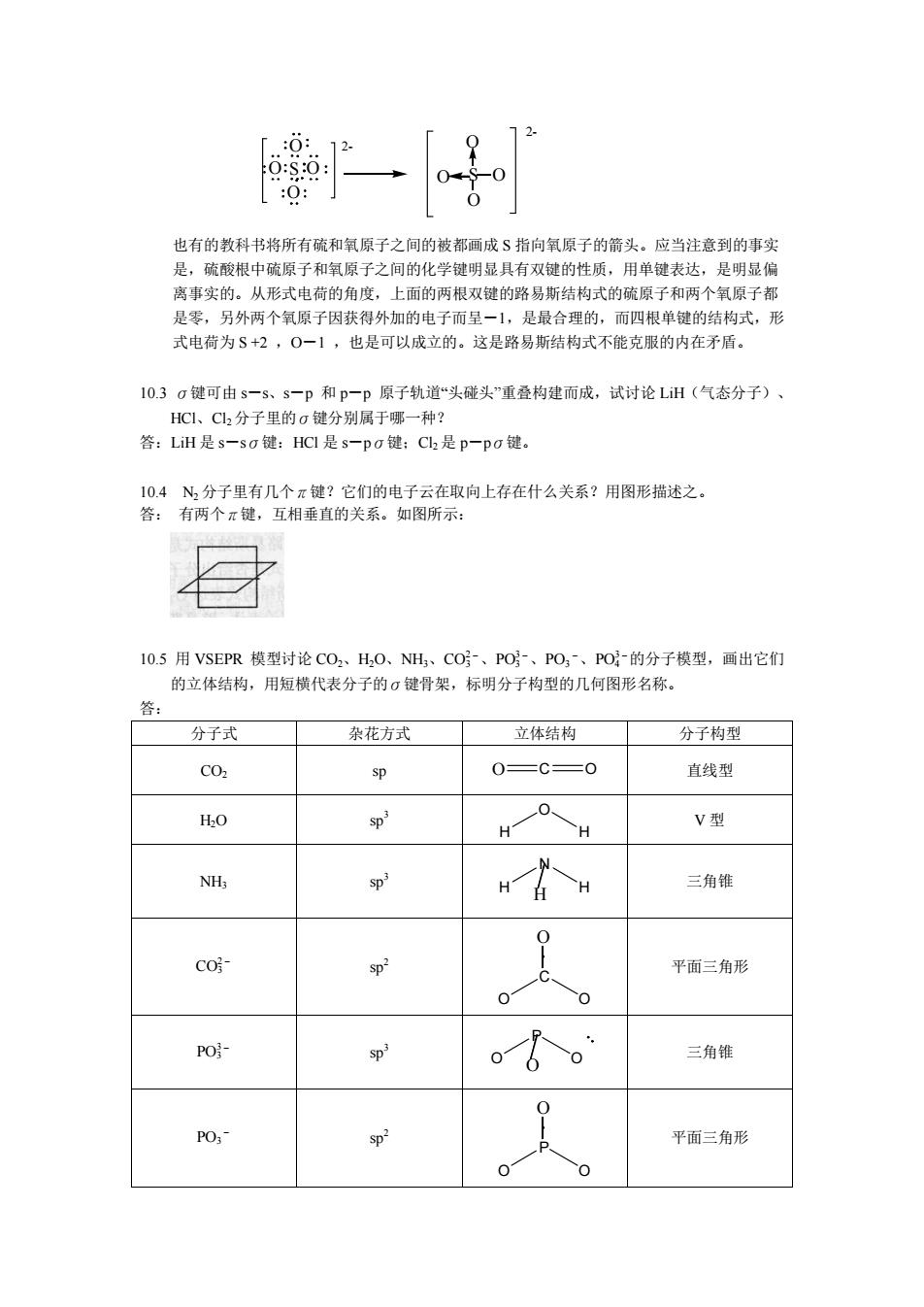
一 也有的教科书将所有硫和氧原子之间的被都画成S指向氧原子的箭头。应当注意到的事实 是,使酸根中硫原子和氧原子之间的化学键明显具有双键的性质,用单键表达,是明显馆 离事实的。从形式电荷的角度,上面的两根双键的路易斯结构式的硫原子和两个氧原子都 是零,另外两个氧原子因获得外加的电子而呈-1,是最合理的而四根单键的结构式。形 式电荷为S+2,O一1,也是可以成立的。这是路易斯结构式不能克服的内在矛盾。 10.3键可由s一s、s一p和p一p原子轨道“头碰头重叠构建而成,试讨论Li训(气态分子) HC、C,分子里的键分别属于哪一种? 答:LiH是s一so健:HCI是s一pG健:C是p一pG键。 0药分子里有几个健?它门的电子云在取向上存在什么关系?用圈形精之 键, 互相垂直的关系。如图所示 10.5用VSEPR模型讨论CO,、H,O、NH,、CO 、PO、PO 、P0的分子模型,画出它们 的立体结构,用短横代表分子的键骨架,标明分子构型的几何图形名称: 答: 分子式 杂花方式 立体结构 分子构型 CO: 0=C=0 直线型 HO sp V型 H H NH, sp 三角锥 co- 平面三角形 0 0 PO 。8o 三角维 0 sp 平面三角形O S O O O 2 S O O O O 2 也有的教科书将所有硫和氧原子之间的被都画成 S 指向氧原子的箭头。应当注意到的事实 是,硫酸根中硫原子和氧原子之间的化学键明显具有双键的性质,用单键表达,是明显偏 离事实的。从形式电荷的角度,上面的两根双键的路易斯结构式的硫原子和两个氧原子都 是零,另外两个氧原子因获得外加的电子而呈-1,是最合理的,而四根单键的结构式,形 式电荷为 S +2 ,O-1 ,也是可以成立的。这是路易斯结构式不能克服的内在矛盾。 10.3 σ键可由 s-s、s-p 和 p-p 原子轨道“头碰头”重叠构建而成,试讨论 LiH(气态分子)、 HCl、Cl2分子里的σ键分别属于哪一种? 答:LiH 是 s-sσ键:HCl 是 s-pσ键;Cl2 是 p-pσ键。 10.4 N2 分子里有几个π键?它们的电子云在取向上存在什么关系?用图形描述之。 答: 有两个π键,互相垂直的关系。如图所示: 10.5 用 VSEPR 模型讨论 CO2、H2O、NH3、CO3 2- 、PO3 3- 、PO3- 、PO4 3- 的分子模型,画出它们 的立体结构,用短横代表分子的σ键骨架,标明分子构型的几何图形名称。 答: 分子式 杂花方式 立体结构 分子构型 CO2 sp O C O 直线型 H2O sp 3 O H H V 型 NH3 sp 3 N H H H 三角锥 CO3 2- sp 2 C O O O 平面三角形 PO3 3- sp 3 P O O O 三角锥 PO3- sp 2 P O O O 平面三角形