正在加载图片...
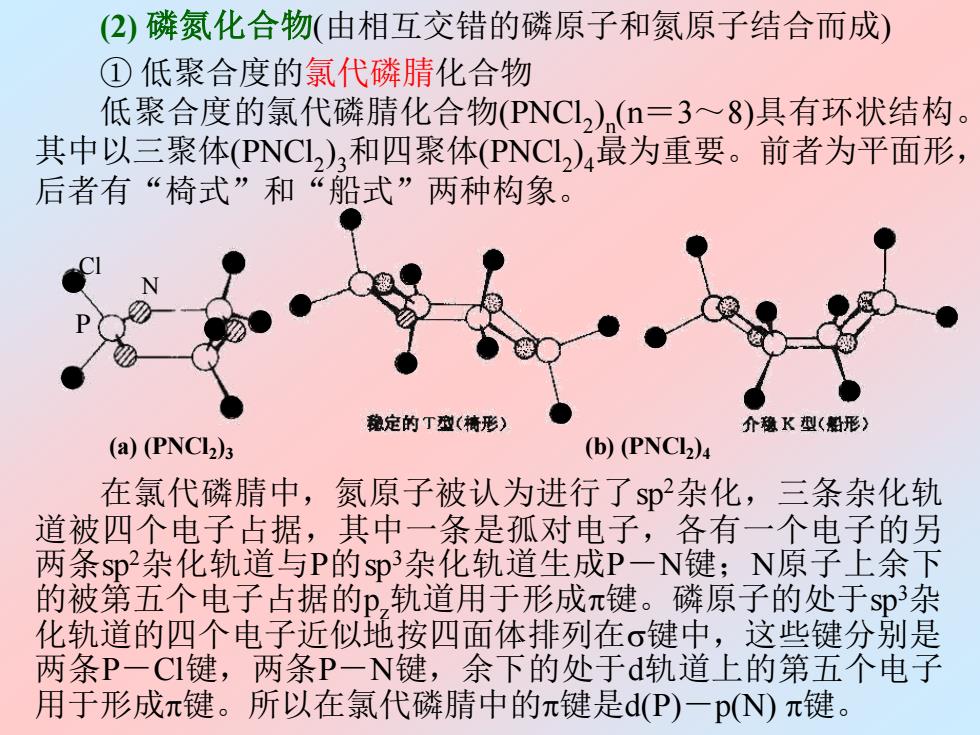
(2)磷氮化合物(由相互交错的磷原子和氮原子结合而成) ①低聚合度的氯代磷腈化合物 低聚合度的氯代磷睛化合物(PNC12)(n=3~8)具有环状结构。 其中以三聚体(PNCL2)3和四聚体(PNCL)4最为重要。前者为平面形, 后者有“椅式”和“船式”两种构象。 魏定的丁型(墙形) 介稳K型(船形) (a)(PNCI)3 (b)(PNCI) 在氯代磷腈中,氮原子被认为进行了$p杂化,三条杂化轨 道被四个电子占据,其中一条是孤对电子,各有一个电子的另 两条sp杂化轨道与P的sp3杂化轨道生成P一N键;N原子上余下 的被第五个电子占据的p,轨道用于形成π键。磷原子的处于sp杂 化轨道的四个电子近似地按四面体排列在σ键中,这些键分别是 两条P一CI键,两条P一N键,余下的处于d轨道上的第五个电子 用于形成π键。所以在氯代磷腈中的π键是d(P)一p(N)π键。(2) 磷氮化合物(由相互交错的磷原子和氮原子结合而成) ① 低聚合度的氯代磷腈化合物 低聚合度的氯代磷腈化合物(PNCl2 ) n (n=3~8)具有环状结构。 其中以三聚体(PNCl2 ) 3和四聚体(PNCl2 ) 4最为重要。前者为平面形, 后者有“椅式”和“船式”两种构象。 (b) (PNCl2 )4 (a) (PNCl2 )3 P Cl N 在氯代磷腈中,氮原子被认为进行了sp2杂化,三条杂化轨 道被四个电子占据,其中一条是孤对电子,各有一个电子的另 两条sp2杂化轨道与P的sp3杂化轨道生成P-N键;N原子上余下 的被第五个电子占据的pz轨道用于形成键。磷原子的处于sp3杂 化轨道的四个电子近似地按四面体排列在键中,这些键分别是 两条P-Cl键,两条P-N键,余下的处于d轨道上的第五个电子 用于形成键。所以在氯代磷腈中的键是d(P)-p(N) 键