正在加载图片...
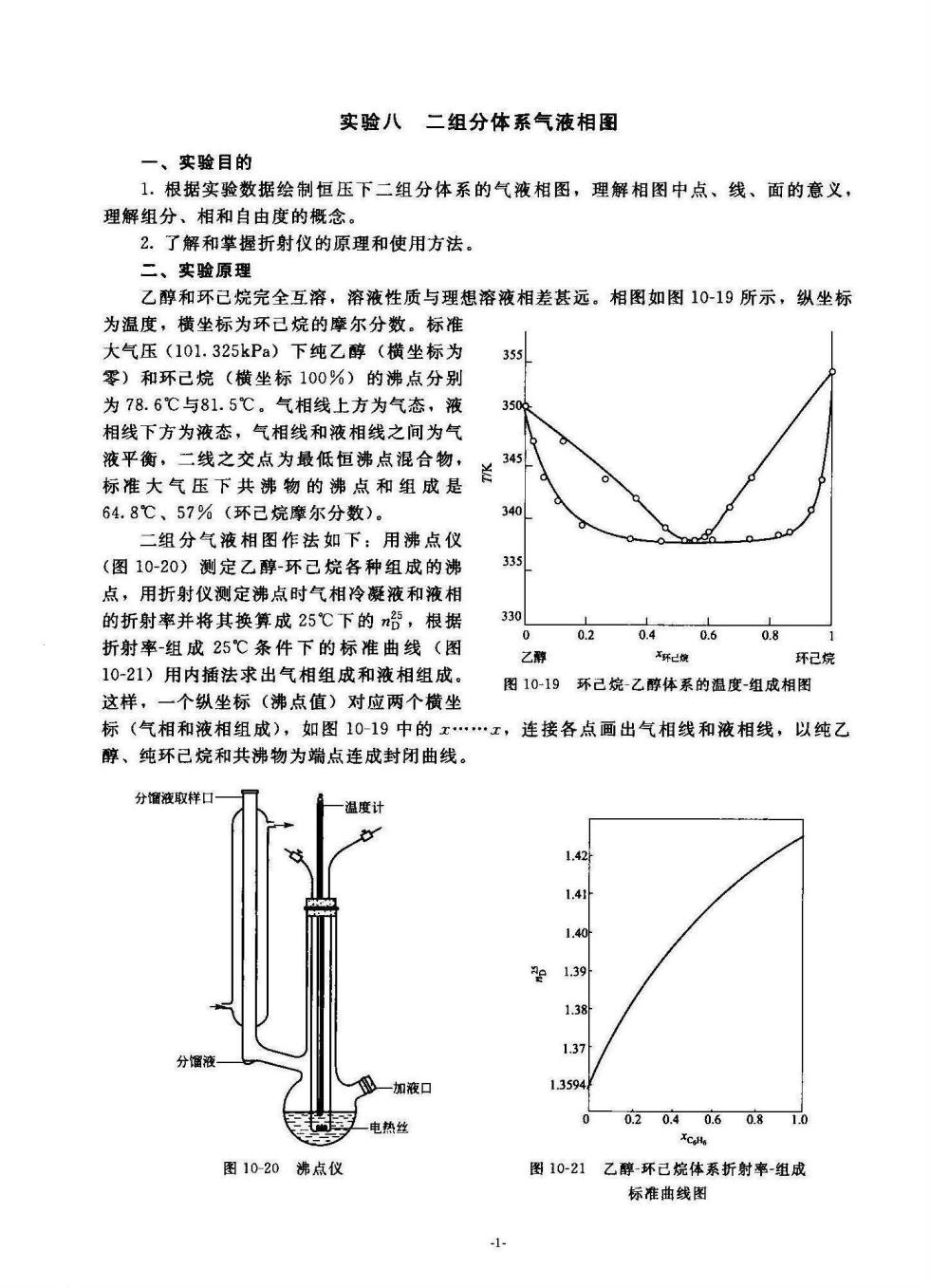
实验八二组分体系气液相图 一、实验目的 1.根据实验数据绘制恒压下二组分体系的气液相图,理解相图中点、线、面的意义, 理解组分、相和自由度的概念。 2.了解和举握折射仪的原理和使用方法。 二、实验原理 乙醇和环己烷完全互溶,溶液性质与理想溶液相差甚远。相图如图10-19所示,纵坐标 为温度,横坐标为环己烷的摩尔分数。标准 大气压(101.325kPa)下纯乙醇(横坐标为 355 零)和环己烷(横坐标100%)的沸点分别 为78.6℃与81.5℃。气相线上方为气态,液 相线下方为液态,气相线和液相线之间为气 液平衡,二线之交点为最低恒沸点混合物, 345 标准大气压下共沸物的沸点和组成是 64.8℃、57%(环己烷摩尔分数)。 340 二组分气液相图作法如下:用沸点仪 (图10-20)测定乙醇-环己烷各种组成的沸 335 点,用折射仪测定沸点时气相冷凝液和液相 的折射率并将其换算成25℃下的n,根据 0 0.20.40.60.8 折射率-组成25℃条件下的标准曲线(图 乙醇 x纸能 环己 10-21)用内插法求出气相组成和液相组成。 图10-19环己烷-乙醇体系的温度-组成相图 这样,一个纵坐标(沸点值)对应两个横坐 标(气相和液相组成),如图10-19中的x…x,连接各点画出气相线和液相线,以纯乙 醇、纯环己烷和共沸物为端点连成封闭曲线。 分液取样口 一温度计 1.4 1.41 1.39 1.38 137 分液 一加液口 13594 一电热约 0020.40.60810 图1020沸点仪 图1021乙醇-环己烷体系折射率-组成 标准曲线图