正在加载图片...
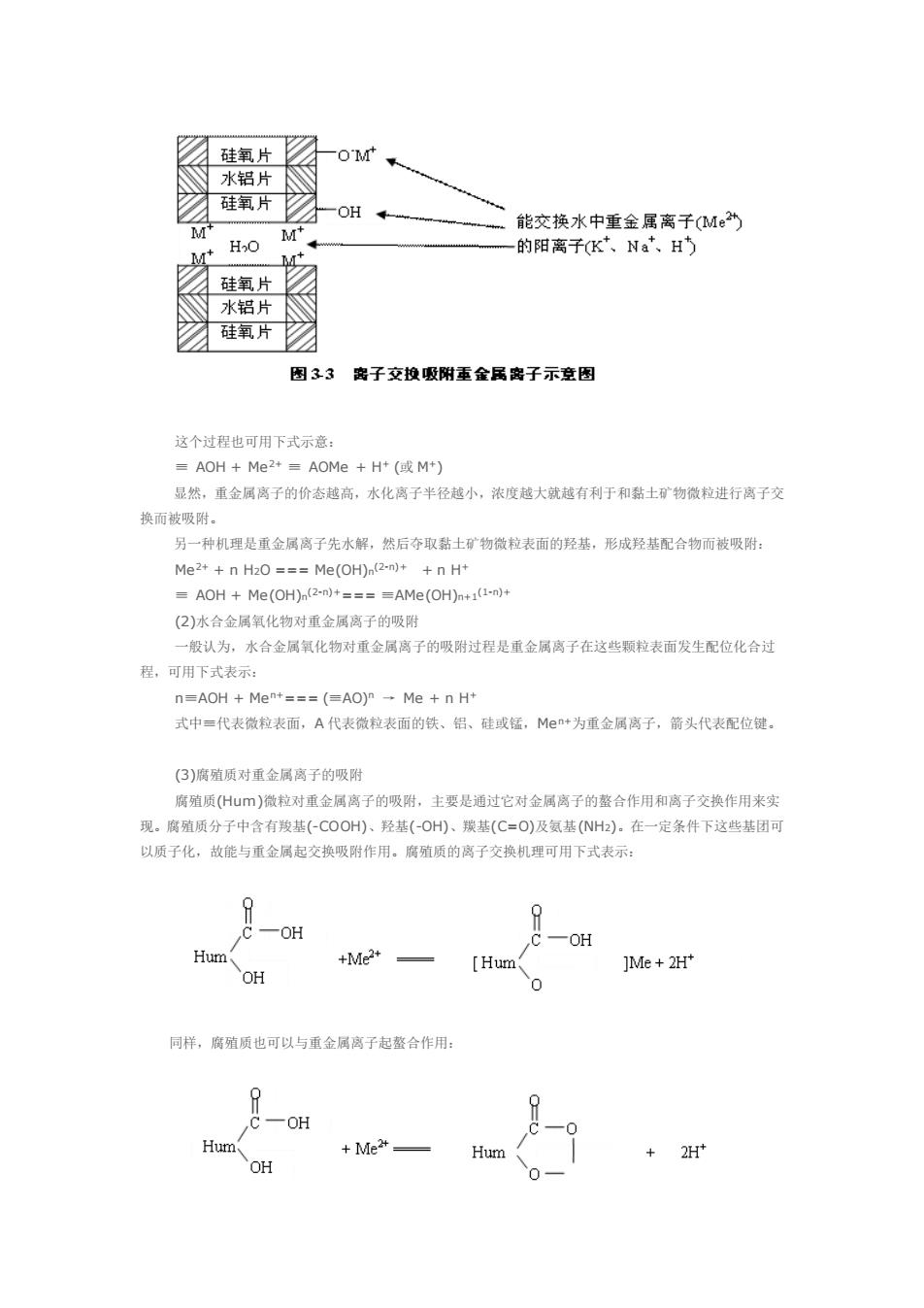
硅氧片 -OM 的水铝片 硅氧片 -OH+ 能交筷水中重金属离子(M” M -的阳离子K,Na、H M" 硅氧片 水铝片 硅氧片☑ 图33 密子交投吸附重金属离子示图 这个过程也可用下式示意: AOH+Me+=AOMe +H(M) 显然,重金属离子的价态越高,水化高子半径越小,浓度越大就越有利于和黏士矿物微粒进行离子交 换而被吸附 另一种机理是重金属离子先水解,然后夺取黏士矿物微粒表而的羟基,形成羟基配合物而被吸附: Me++n H2O===Me(OH)n(-)++n H* =AOH+Me(OH)(2m)+====AMe(OH)+1() (2)水合金属氧化物对重金属离子的吸附 一般认为,水合金属氧化物对重金属离子的吸附过程是重金属离子在这些颗粒表面发生配位化合过 程,可用下式表示 n=AOH Me+===(=AO)-Me n H* 式中=代表微粒表面,A代表微粒表面的铁、铝、硅或锰,M+为重金属离子,箭头代表配位键。 (3)腐殖质对重金属离子的吸附 腐殖质(H山m)微拉对重金属离子的吸附,主要是通过它对金属离子的整合作用和离子交换作用来实 现。腐殖质分子中含有羧基(-COOH)、羟基(-O)、基(C=O)及氨基(NH),在一定条件下这些基团可 以质子化,故能与重金属起交换吸附作用。腐殖质的离子交换机理可用下式表示 一0H Hum +Me2+ [Hum ]Me+2H OH 问样,腐殖质也可以与重金属离子起整合作用: -OH Hu 2H OH 这个过程也可用下式示意: ≡ AOH + Me2+ ≡ AOMe + H+ (或 M+) 显然,重金属离子的价态越高,水化离子半径越小,浓度越大就越有利于和黏土矿物微粒进行离子交 换而被吸附。 另一种机理是重金属离子先水解,然后夺取黏土矿物微粒表面的羟基,形成羟基配合物而被吸附: Me2+ + n H2O === Me(OH)n (2-n)+ + n H+ ≡ AOH + Me(OH)n (2-n)+=== ≡AMe(OH)n+1(1-n)+ (2)水合金属氧化物对重金属离子的吸附 一般认为,水合金属氧化物对重金属离子的吸附过程是重金属离子在这些颗粒表面发生配位化合过 程,可用下式表示: n≡AOH + Men+=== (≡AO)n → Me + n H+ 式中≡代表微粒表面,A 代表微粒表面的铁、铝、硅或锰,Men+为重金属离子,箭头代表配位键。 (3)腐殖质对重金属离子的吸附 腐殖质(Hum)微粒对重金属离子的吸附,主要是通过它对金属离子的螯合作用和离子交换作用来实 现。腐殖质分子中含有羧基(-COOH)、羟基(-OH)、羰基(C=O)及氨基(NH2)。在一定条件下这些基团可 以质子化,故能与重金属起交换吸附作用。腐殖质的离子交换机理可用下式表示: 同样,腐殖质也可以与重金属离子起螯合作用: