正在加载图片...
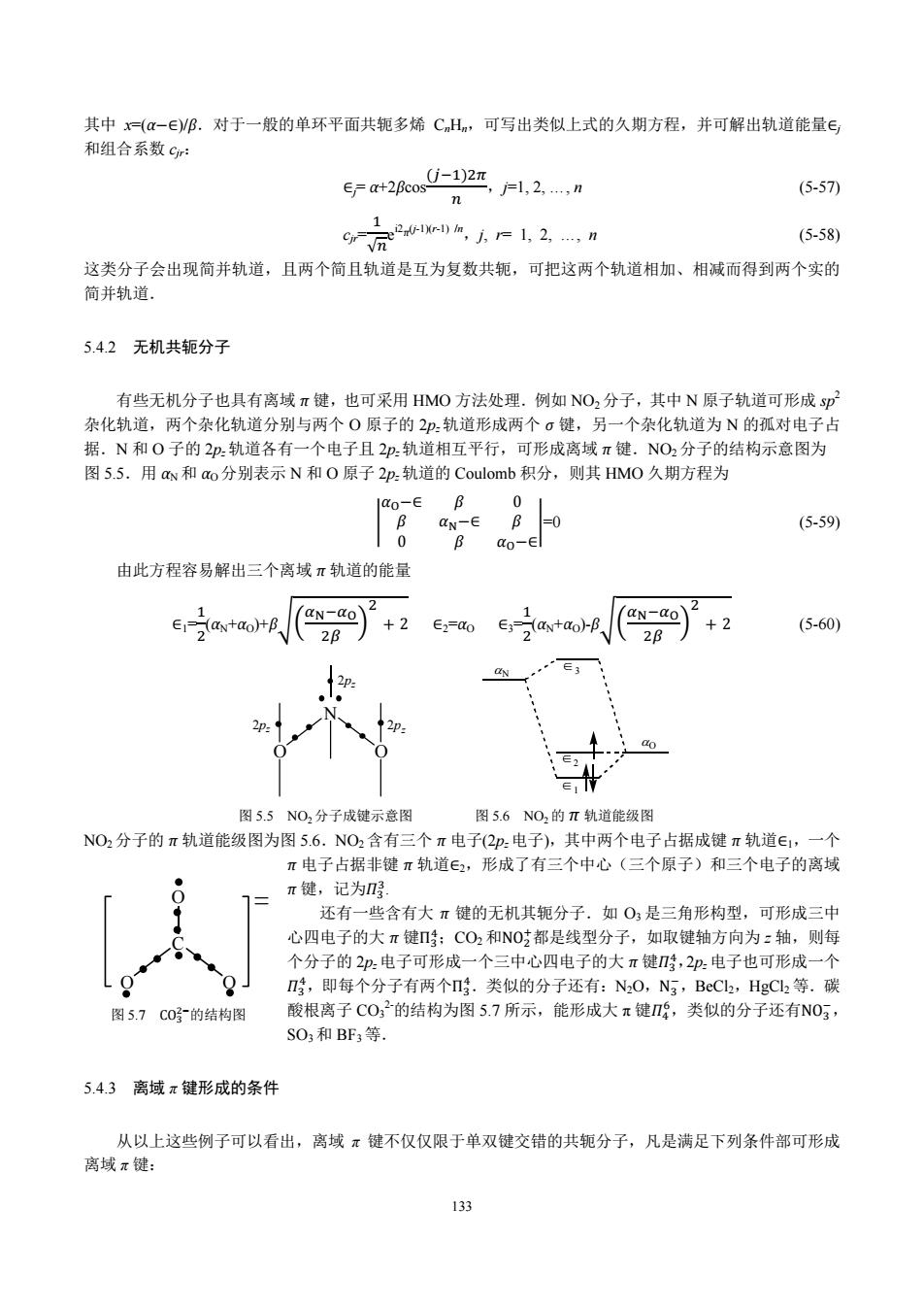
其中x=(a-∈)B.对于一般的单环平面共轭多烯CmH,可写出类似上式的久期方程,并可解出轨道能量∈ 和组合系数cr: ∈=a+2fcos j-1)2π =1,2,…,n (5-57) =2m,方,=1,2,,n c in (5-58) 这类分子会出现简并轨道,且两个简且轨道是互为复数共轭,可把这两个轨道相加、相减而得到两个实的 简并轨道. 5.4.2无机共轭分子 有些无机分子也具有离域π键,也可采用HMO方法处理.例如NO2分子,其中N原子轨道可形成sp 杂化轨道,两个杂化轨道分别与两个O原子的2.轨道形成两个σ键,另一个杂化轨道为N的孤对电子占 据.N和O子的2p轨道各有一个电子且2轨道相互平行,可形成离域π键.NO2分子的结构示意图为 图5.5.用aw和ao分别表示N和O原子2p.轨道的Coulomb积分,则其HMO久期方程为 Qo-E B 0 B aN-E (5-59) 0 B o-∈l 由此方程容易解出三个离域π轨道的能量 2 aN-dO +2 E3->(ax+ao)-B aN-QO ∈12 +B、 +2 2B 2B (5-60) N 图5.5NO,分子成键示意图 图5.6NO,的π轨道能级图 NO2分子的π轨道能级图为图5.6.NO2含有三个π电子(2p:电子),其中两个电子占据成键π轨道∈1,一个 π电子占据非键π轨道E2,形成了有三个中心(三个原子)和三个电子的离域 π键,记为 还有一些含有大π键的无机其轭分子.如O,是三角形构型,可形成三中 心四电子的大π键n;CO2和NO都是线型分子,如取键轴方向为:轴,则每 个分子的2p.电子可形成一个三中心四电子的大π键,2p.电子也可形成一个 ,即每个分子有两个.类似的分子还有:N2O,N3,BeCl2,HgC2等.碳 图5.7C0号的结构图 酸根离子CO32的结构为图5.7所示,能形成大π键Π,类似的分子还有N03, SO3和BF3等. 5.4.3离域π键形成的条件 从以上这些例子可以看出,离域π键不仅仅限于单双键交错的共轭分子,凡是满足下列条件部可形成 离域π键: 133133 其中 x=(αെ∈)/β.对于一般的单环平面共轭多烯 CnHn,可写出类似上式的久期方程,并可解出轨道能量∈j 和组合系数 cjr: ∈j= α+2βcos ሺିଵሻଶగ ,j=1, 2, …, n (5-57) cjr= ଵ √ e i2π(j-1)(r-1) /n ,j, r= 1, 2, …, n (5-58) 这类分子会出现简并轨道,且两个简且轨道是互为复数共轭,可把这两个轨道相加、相减而得到两个实的 简并轨道. 5.4.2 无机共轭分子 有些无机分子也具有离域 π 键,也可采用 HMO 方法处理.例如 NO2 分子,其中 N 原子轨道可形成 sp 2 杂化轨道,两个杂化轨道分别与两个 O 原子的 2pz 轨道形成两个 σ 键,另一个杂化轨道为 N 的孤对电子占 据.N 和 O 子的 2pz 轨道各有一个电子且 2pz 轨道相互平行,可形成离域 π 键.NO2 分子的结构示意图为 图 5.5.用 αN和 αO分别表示 N 和 O 原子 2pz 轨道的 Coulomb 积分,则其 HMO 久期方程为 อ 0 ߚ ∋െߙ ߚ ∋െߙ ߚ 0 ߙߚെ∈อ=0 (5-59) 由此方程容易解出三个离域 π 轨道的能量 ∈1= ଵ ଶ (αN+αO)+βටቀ ఈొିఈో ଶఉ ቁ ଶ 2 ∈2=αO ∈3= ଵ ଶ (αN+αO)-βටቀ ఈొିఈో ଶఉ ቁ ଶ 2 (5-60) N O O 2pz 2pz 2pz O N ∈1 ∈2 ∈3 图 5.5 NO2 分子成键示意图 图 5.6 NO2 的 π 轨道能级图 NO2 分子的 π 轨道能级图为图 5.6.NO2 含有三个 π 电子(2pz 电子),其中两个电子占据成键 π 轨道∈1,一个 π 电子占据非键 π 轨道∈2,形成了有三个中心(三个原子)和三个电子的离域 π 键,记为ߎଷ ଷ. 还有一些含有大 π 键的无机其轭分子.如 O3 是三角形构型,可形成三中 心四电子的大 π 键Πଷ ସ ;CO2 和NOଶ ା都是线型分子,如取键轴方向为 z 轴,则每 个分子的 2pz电子可形成一个三中心四电子的大 π 键ߎଷ ସ,2pz 电子也可形成一个 ଷߎ ସ,即每个分子有两个Πଷ ସ.类似的分子还有:N2O,Nଷ ି,BeCl2,HgCl2 等.碳 酸根离子 CO3 2-的结构为图 5.7 所示,能形成大 π 键ߎସ ,类似的分子还有NOଷ ି, SO3 和 BF3 等. 5.4.3 离域 π 键形成的条件 从以上这些例子可以看出,离域 π 键不仅仅限于单双键交错的共轭分子,凡是满足下列条件部可形成 离域 π 键: 图 5.7 COଷ ଶି的结构图 C O O O