正在加载图片...
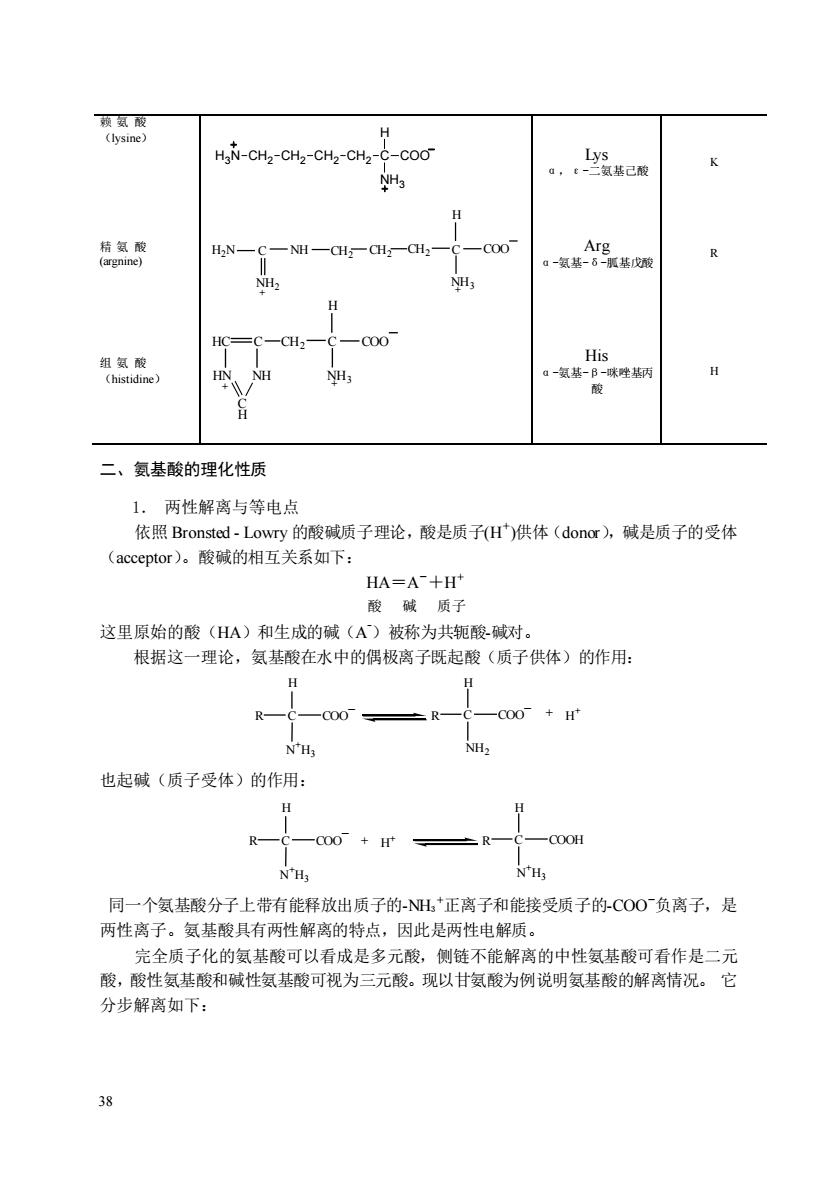
HaN-CH2-CH2-CHz-CH2-C-COO N NHs 。,己 HN- 一NH一CH一CH一aH -c00 CH. -00 -氨 二、氨基酸的理化性质 1.两性解离与等电点 依照Bronsted-Lowry的酸碱质子理论,酸是质子(H)供体(donor),碱是质子的受体 (acceptor)。酸碱的相互关系如下: HA=A十H 酸碱质子 这里原始的酸(HA)和生成的碱(A)被称为共轭酸碱对。 根据这一理论,氨基酸在水中的偶极离子既起酸(质子供体)的作用: H 00+H nH NH2 也起碱(质子受体)的作用: R 000H N'Hg 同一个氨基酸分子上带有能释放出质子的H正离子和能接受质子的CO0负离子,是 两性离子。氨基酸具有两性解离的特点,因此是两性电解质。 完全质子化的氨基酸可以看成是多元酸,侧链不能解离的中性氨基酸可看作是二元 酸,酸性氨基酸和碱性氨基酸可视为三元酸。现以甘氨酸为例说明氨基酸的解离情况。它 分步解离如下:38 赖 氨 酸 (lysine) Lys α,ε-二氨基己酸 K 精 氨 酸 (argnine) + CH2 C H NH3 CH CH2 COO C NH 2 NH2 H2N + Arg α-氨基-δ-胍基戊酸 R 组 氨 酸 (histidine) + CH2 C H NH3 HC C COO HN NH + C H His α-氨基-β-咪唑基丙 酸 H 二、氨基酸的理化性质 1. 两性解离与等电点 依照 Bronsted - Lowry 的酸碱质子理论,酸是质子(H+ )供体(donor),碱是质子的受体 (acceptor)。酸碱的相互关系如下: HA=A -+H + 酸 碱 质子 这里原始的酸(HA)和生成的碱(A -)被称为共轭酸-碱对。 根据这一理论,氨基酸在水中的偶极离子既起酸(质子供体)的作用: R C H N +H3 COO _ NH2 + H + R C H COO _ 也起碱(质子受体)的作用: R C H N +H3 COO _ N +H3 + H + R C H COOH 同一个氨基酸分子上带有能释放出质子的-NH3 +正离子和能接受质子的-COO-负离子,是 两性离子。氨基酸具有两性解离的特点,因此是两性电解质。 完全质子化的氨基酸可以看成是多元酸,侧链不能解离的中性氨基酸可看作是二元 酸,酸性氨基酸和碱性氨基酸可视为三元酸。现以甘氨酸为例说明氨基酸的解离情况。 它 分步解离如下: C H COO NH3 H3N CH2 CH2 CH2 CH2