正在加载图片...
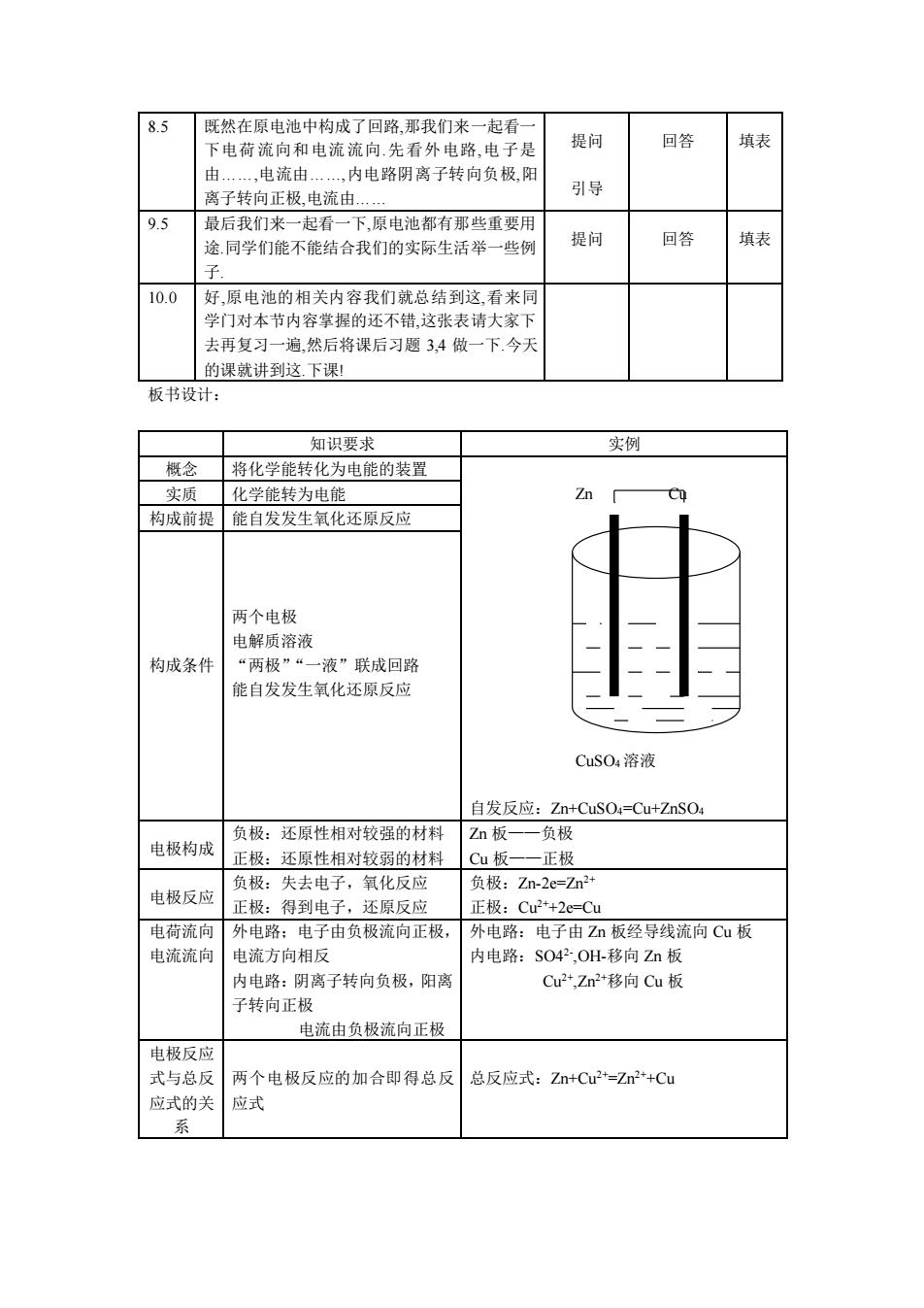
8.5 再姚在原申油中构成了回路那我们来一起看一 下电荷流向和电流流向先看外电路,电子是 提问 回答 填表 ,电流由 ,内电路阴离子转向负极阳 离子转向正极电流由. 引导 9.5 最后我们来一起看一下,原电池都有那些重要用 途.同学们能不能结合我们的实际生活举一些例 提问 回答 填表 10.0 好,原电池的相关内容我们就总结到这,看来同 学门对本节内容掌握的还不错,这张表请大家下 去再复习一遍,然后将课后习题3,4做一下今天 的课就讲到这.下课! 板书设计: 知识要求 实例 今 将化学能转化为电能的装置 实质化学能转为电能 n 构成前提能自发发生氧化还原反应 两个电极 电解质溶液 构成条件 “两极”“一液”联成回路 能自发发生氧化还原反应 CuSO,溶液 自发反应:Zn+CuSO4=Cu+ZnSO4 负极。还厦性相对时较品的材料 Zn板一一负极 电极构成正极:还原性相对较弱的材料 C板一一正极 负极:失去电子,氧化反应 电极反应 负极 Zn-2e=Zn2 正极:得到电子,还原反应 正极:Cu2+2e=Cu 电荷流向外电路:电子由负极流向正极, 外电路:电子由Z小板经导线流向Cu板 电流流向 申流方向相反 内电路:S042,OH-移向Zn板 内电路:阴离子转向负极,阳离 Cu2,Zm2*移向Cu板 子转向 电流由负极流向正极 电极反应 式与总反 两个电极反应的加合即得总反 总反应式:Zn+Cu2=Zr2*+Cu 应式的关 应式 系8.5 既然在原电池中构成了回路,那我们来一起看一 下电荷流向和电流流向.先看外电路,电子是 由.,电流由.,内电路阴离子转向负极,阳 离子转向正极,电流由. 提问 引导 回答 填表 9.5 最后我们来一起看一下,原电池都有那些重要用 途.同学们能不能结合我们的实际生活举一些例 子. 提问 回答 填表 10.0 好,原电池的相关内容我们就总结到这,看来同 学门对本节内容掌握的还不错,这张表请大家下 去再复习一遍,然后将课后习题 3,4 做一下.今天 的课就讲到这.下课! 板书设计: 知识要求 实例 概念 将化学能转化为电能的装置 Zn Cu CuSO4 溶液 自发反应:Zn+CuSO4=Cu+ZnSO4 实质 化学能转为电能 构成前提 能自发发生氧化还原反应 构成条件 两个电极 电解质溶液 “两极”“一液”联成回路 能自发发生氧化还原反应 电极构成 负极:还原性相对较强的材料 正极:还原性相对较弱的材料 Zn 板——负极 Cu 板——正极 电极反应 负极:失去电子,氧化反应 正极:得到电子,还原反应 负极:Zn-2e=Zn2+ 正极:Cu2++2e=Cu 电荷流向 电流流向 外电路;电子由负极流向正极, 电流方向相反 内电路:阴离子转向负极,阳离 子转向正极 电流由负极流向正极 外电路:电子由 Zn 板经导线流向 Cu 板 内电路:SO42- ,OH-移向 Zn 板 Cu2+,Zn2+移向 Cu 板 电极反应 式与总反 应式的关 系 两个电极反应的加合即得总反 应式 总反应式:Zn+Cu2+=Zn2++Cu