正在加载图片...
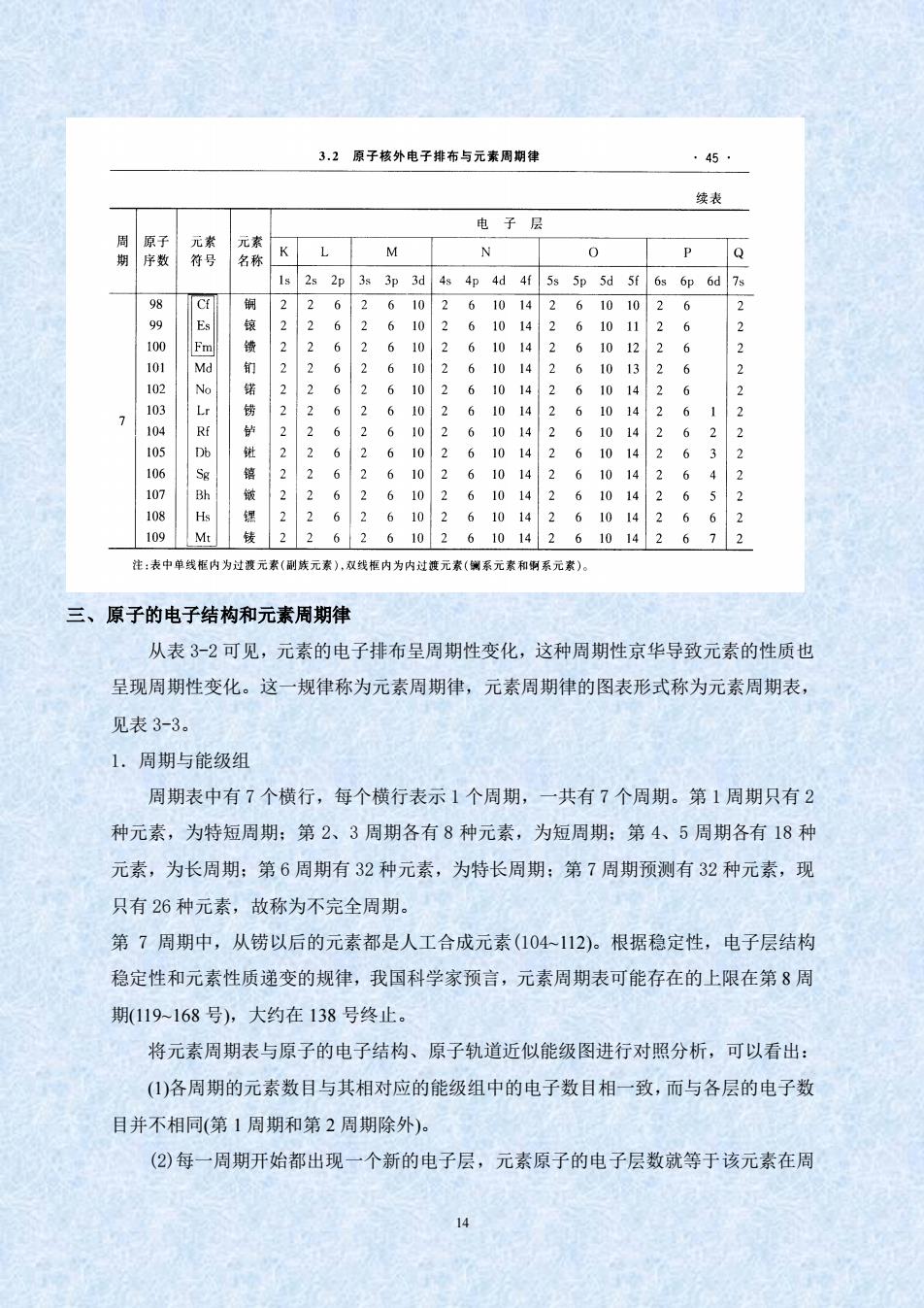
3.2原子核外电子排布与元素周期律 ·45 续表 电子层 1s 2s 2p 3s 3p 3d 4s 4p 4d 4f 5s 5p 5d 5f 6s 6p 6d 78 98 1026101426101026 102610142 6101126 En 22 102610142 6101226 22 1026101426101326 1026101426101426 L 10 2610142610142612 X C 610142610142622 。到 261014 22 261014 注:表中单线框内为过夏元素(副峡元素),双线框内为内过挂元素(侧系元素和期系元素)。 三、原子的电子结构和元素周期律 从表3-2可见,元素的电子排布呈周期性变化,这种周期性京华导致元素的性质也 呈现周期性变化。这一规律称为元素周期律,元素周期律的图表形式称为元素周期表, 见表3-3。 1.周期与能级组 周期表中有7个横行,每个横行表示1个周期,一共有7个周期。第1周期只有2 种元素,为特短周期:第2、3周期各有8种元素,为短周期:第4、5周期各有18种 元素,为长周期:第6周期有32种元素,为特长周期:第7周期预测有32种元素,现 只有26种元素,故称为不完全周期。 第7周期中,从铹以后的元素都是人工合成元素(104112)。根据稳定性,电子层结构 稳定性和元素性质递变的规律,我国科学家预言,元素周期表可能存在的上限在第8周 期(119-168号),大约在138号终止。 将元素周期表与原子的电子结构、原子轨道近似能级图进行对照分析,可以看出: (1)各周期的元素数目与其相对应的能级组中的电子数目相一致,而与各层的电子数 目并不相同(第1周期和第2周期除外)。 (2)每一周期开始都出现一个新的电子层,元素原子的电子层数就等于该元素在周 14 三、原子的电子结构和元素周期律 从表 3-2 可见,元素的电子排布呈周期性变化,这种周期性京华导致元素的性质也 呈现周期性变化。这一规律称为元素周期律,元素周期律的图表形式称为元素周期表, 见表 3-3。 1.周期与能级组 周期表中有 7 个横行,每个横行表示 1 个周期,一共有 7 个周期。第 1 周期只有 2 种元素,为特短周期;第 2、3 周期各有 8 种元素,为短周期;第 4、5 周期各有 18 种 元素,为长周期;第 6 周期有 32 种元素,为特长周期;第 7 周期预测有 32 种元素,现 只有 26 种元素,故称为不完全周期。 第 7 周期中,从铹以后的元素都是人工合成元素(104~112)。根据稳定性,电子层结构 稳定性和元素性质递变的规律,我国科学家预言,元素周期表可能存在的上限在第 8 周 期(119~168 号),大约在 138 号终止。 将元素周期表与原子的电子结构、原子轨道近似能级图进行对照分析,可以看出: (1)各周期的元素数目与其相对应的能级组中的电子数目相一致,而与各层的电子数 目并不相同(第 1 周期和第 2 周期除外)。 (2)每一周期开始都出现一个新的电子层,元素原子的电子层数就等于该元素在周