正在加载图片...
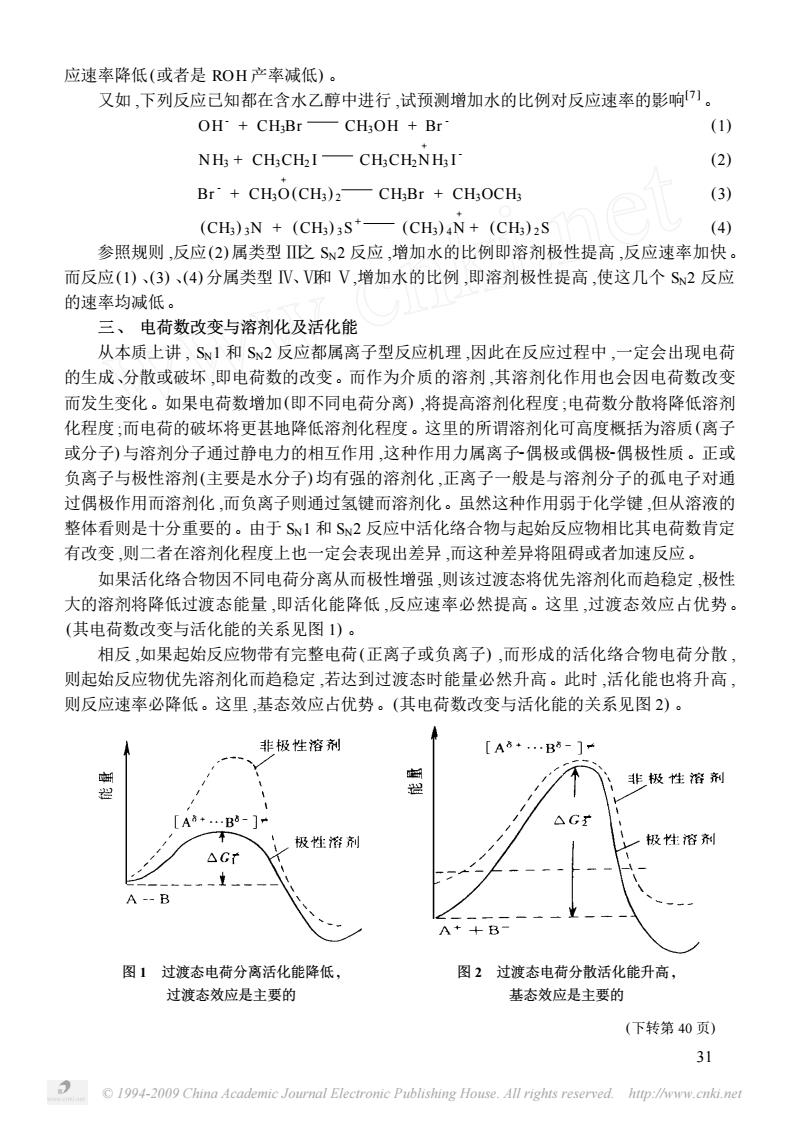
应速率降低(或者是ROH产率减低)」 又如,下列反应已知都在含水乙醇中进行,试预测增加水的比例对反应速率的影响]。 OH+CHBr—CH,OH+Br (1) NH+CHCH2I—CHCH2NHI (2) Br+CH;O(CH3)2-CH;Br CH:OCH; (3) (CH)N (CH)3S*-(CH)aN+(CHs)2S 多 参照规则,反应(2)属类型戊S2反应,增加水的比例即溶剂极性提高,反应速率加快。 而反应(I)、(3)、(4)分属类型V、V和V,增加水的比例,即溶剂极性提高,使这几个S2反应 的速率均减低。 三、电荷数改变与溶剂化及活化能 从本质上讲,S1和S2反应都属离子型反应机理,因此在反应过程中,一定会出现电荷 的生成、分散或破坏,即电荷数的改变。而作为介质的溶剂,其溶剂化作用也会因电荷数改变 而发生变化。如果电荷数增加(即不同电荷分离),将提高溶剂化程度;电荷数分散将降低溶剂 化程度:而电荷的破坏将更甚地降低溶剂化程度。这里的所谓溶剂化可高度概括为溶质(离子 或分子)与溶剂分子通过静电力的相互作用,这种作用力属离子偶极或偶极偶极性质。正或 负离子与极性溶剂(主要是水分子)均有强的溶剂化,正离子一般是与溶剂分子的孤电子对通 过偶极作用而溶剂化,而负离子则通过氢键而溶剂化。虽然这种作用弱于化学键,但从溶液的 整体看则是十分重要的。由于S1和S2反应中活化络合物与起始反应物相比其电荷数肯定 有改变则二者在溶剂化程度上也一定会表现出差异,而这种差异将阻碍或者加速反应。 如果活化络合物因不同电荷分离从而极性增强,则该过渡态将优先溶剂化而趋稳定,极性 大的溶剂将降低过渡态能量,即活化能降低,反应速率必然提高。这里,过渡态效应占优势 (其电荷数改变与活化能的关系见图1)。 相反,如果起始反应物带有完整电荷(正离子或负离子),而形成的活化络合物电荷分散, 则起始反应物优先溶剂化而趋稳定,若达到过渡态时能量必然升高。此时,活化能也将升高 则反应速率必降低。这里,基态效应占优势。(其电荷数改变与活化能的关系见图2)。 非极性溶剂 [A8…B-1- 非极性溶剂 [A8+…B5-]- 极性溶剂 极性溶剂 △G· 图1过渡态电荷分离活化能降低, 图2过波态电荷分散活化能升高, 过渡态效应是主要的 基态效应是主要的 (下转第40页) 31 94-2009 China Academic Journal Electronie Publishing House.All righis reserved.htp://ww.cnki.ne© 1994-2009 China Academic Journal Electronic Publishing House. All rights reserved. http://www.cnki.net 应速率降低(或者是 ROH 产率减低) 。 又如 ,下列反应已知都在含水乙醇中进行 ,试预测增加水的比例对反应速率的影响[7 ] 。 OH - + CH3Br CH3OH + Br - (1) NH3 + CH3CH2 I CH3CH2N + H3 I - (2) Br - + CH3O + (CH3 ) 2 CH3Br + CH3OCH3 (3) (CH3 ) 3N + (CH3 ) 3S + (CH3 ) 4N + + (CH3 ) 2S (4) 参照规则 ,反应(2) 属类型 Ⅲ之 SN2 反应 ,增加水的比例即溶剂极性提高 ,反应速率加快。 而反应(1) 、(3) 、(4) 分属类型 Ⅳ、Ⅵ和 Ⅴ,增加水的比例 ,即溶剂极性提高 ,使这几个 SN2 反应 的速率均减低。 三、 电荷数改变与溶剂化及活化能 从本质上讲 , SN1 和 SN2 反应都属离子型反应机理 ,因此在反应过程中 ,一定会出现电荷 的生成、分散或破坏 ,即电荷数的改变。而作为介质的溶剂 ,其溶剂化作用也会因电荷数改变 而发生变化。如果电荷数增加(即不同电荷分离) ,将提高溶剂化程度 ;电荷数分散将降低溶剂 化程度 ;而电荷的破坏将更甚地降低溶剂化程度。这里的所谓溶剂化可高度概括为溶质(离子 或分子) 与溶剂分子通过静电力的相互作用 ,这种作用力属离子2偶极或偶极2偶极性质。正或 负离子与极性溶剂(主要是水分子) 均有强的溶剂化 ,正离子一般是与溶剂分子的孤电子对通 过偶极作用而溶剂化 ,而负离子则通过氢键而溶剂化。虽然这种作用弱于化学键 ,但从溶液的 整体看则是十分重要的。由于 SN1 和 SN2 反应中活化络合物与起始反应物相比其电荷数肯定 有改变 ,则二者在溶剂化程度上也一定会表现出差异 ,而这种差异将阻碍或者加速反应。 如果活化络合物因不同电荷分离从而极性增强 ,则该过渡态将优先溶剂化而趋稳定 ,极性 大的溶剂将降低过渡态能量 ,即活化能降低 ,反应速率必然提高。这里 ,过渡态效应占优势。 (其电荷数改变与活化能的关系见图 1) 。 相反 ,如果起始反应物带有完整电荷(正离子或负离子) ,而形成的活化络合物电荷分散 , 则起始反应物优先溶剂化而趋稳定 ,若达到过渡态时能量必然升高。此时 ,活化能也将升高 , 则反应速率必降低。这里 ,基态效应占优势。(其电荷数改变与活化能的关系见图 2) 。 图 1 过渡态电荷分离活化能降低 , 过渡态效应是主要的 图 2 过渡态电荷分散活化能升高 , 基态效应是主要的 (下转第 40 页) 31