正在加载图片...
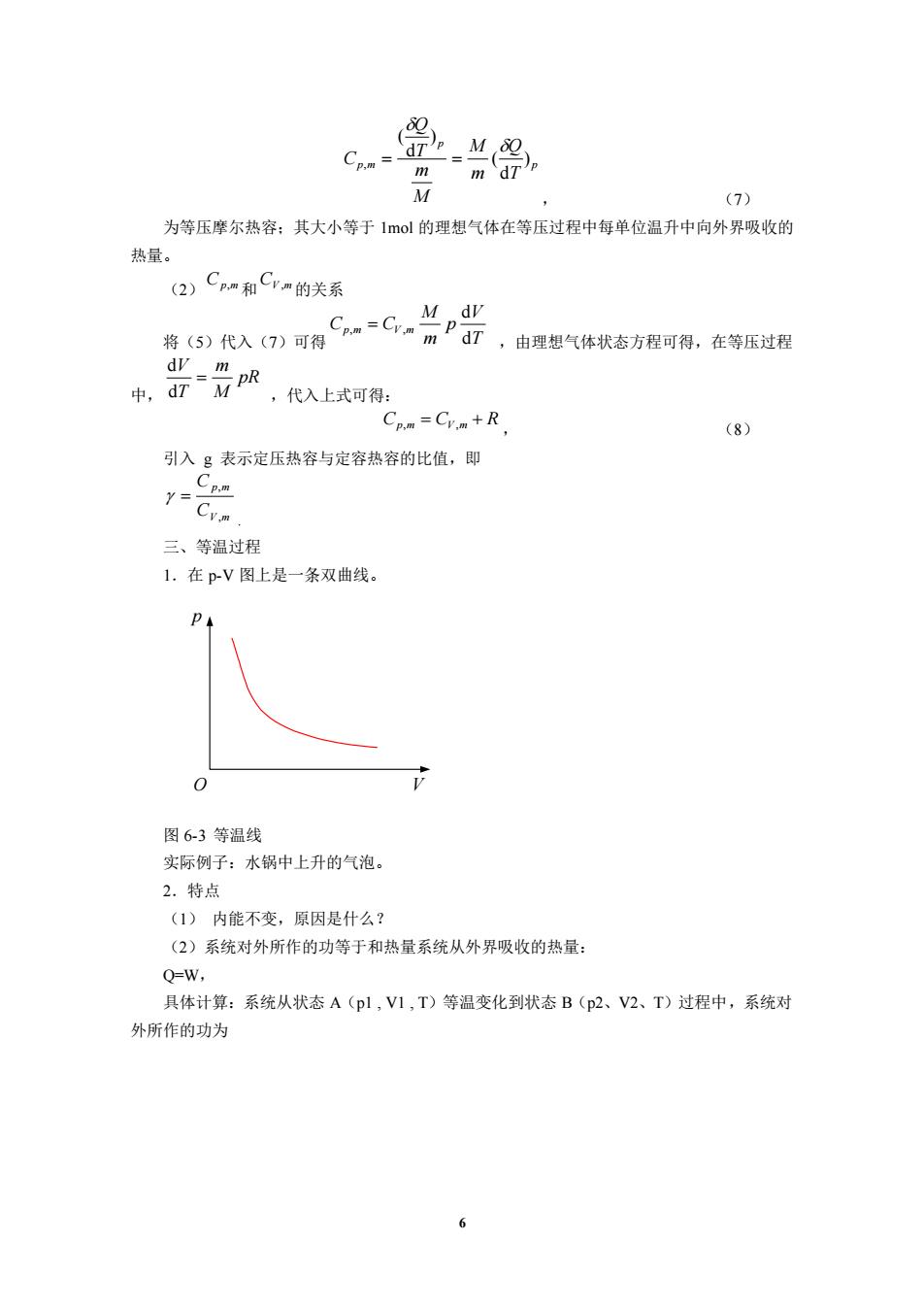
(7) 为等压摩尔热容:其大小等于1ml的理想气体在等压过程中每单位温升中向外界吸收的 热量。 (2)Cpm和Cvm的关系 M dv 将(5)代入(7)可得 mPd7,由理想气体状态方程可得,在等压过程 ,代入上式可得 Cpm Crm+R (8) 引入g表示定压热容与定容热容的比值,即 1-Cvn 三、等温过程 1.在pV图上是一条双曲线。 0 图6-3等温线 实际例子:水锅中上升的气泡。 2.特点 (1)内能不变,原因是什么? (2)系统对外所作的功等于和热量系统从外界吸收的热量: Q=W, 具体计算:系统从状态A(pl,V1,T)等温变化到状态B(p2、V2、T)过程中,系统对 外所作的功为 6 p p p m T Q m M M m T Q C ) d ( ) d ( , = = , (7) 为等压摩尔热容;其大小等于 1mol 的理想气体在等压过程中每单位温升中向外界吸收的 热量。 (2) Cp,m 和 CV ,m 的关系 将(5)代入(7)可得 T V p m M Cp m CV m d d , = , ,由理想气体状态方程可得,在等压过程 中, pR M m T V = d d ,代入上式可得: Cp,m = CV ,m + R , (8) 引入 g 表示定压热容与定容热容的比值,即 V m p m C C , , = . 三、等温过程 1.在 p-V 图上是一条双曲线。 p O V 图 6-3 等温线 实际例子:水锅中上升的气泡。 2.特点 (1) 内能不变,原因是什么? (2)系统对外所作的功等于和热量系统从外界吸收的热量: Q=W, 具体计算:系统从状态 A(p1 , V1 , T)等温变化到状态 B(p2、V2、T)过程中,系统对 外所作的功为