正在加载图片...
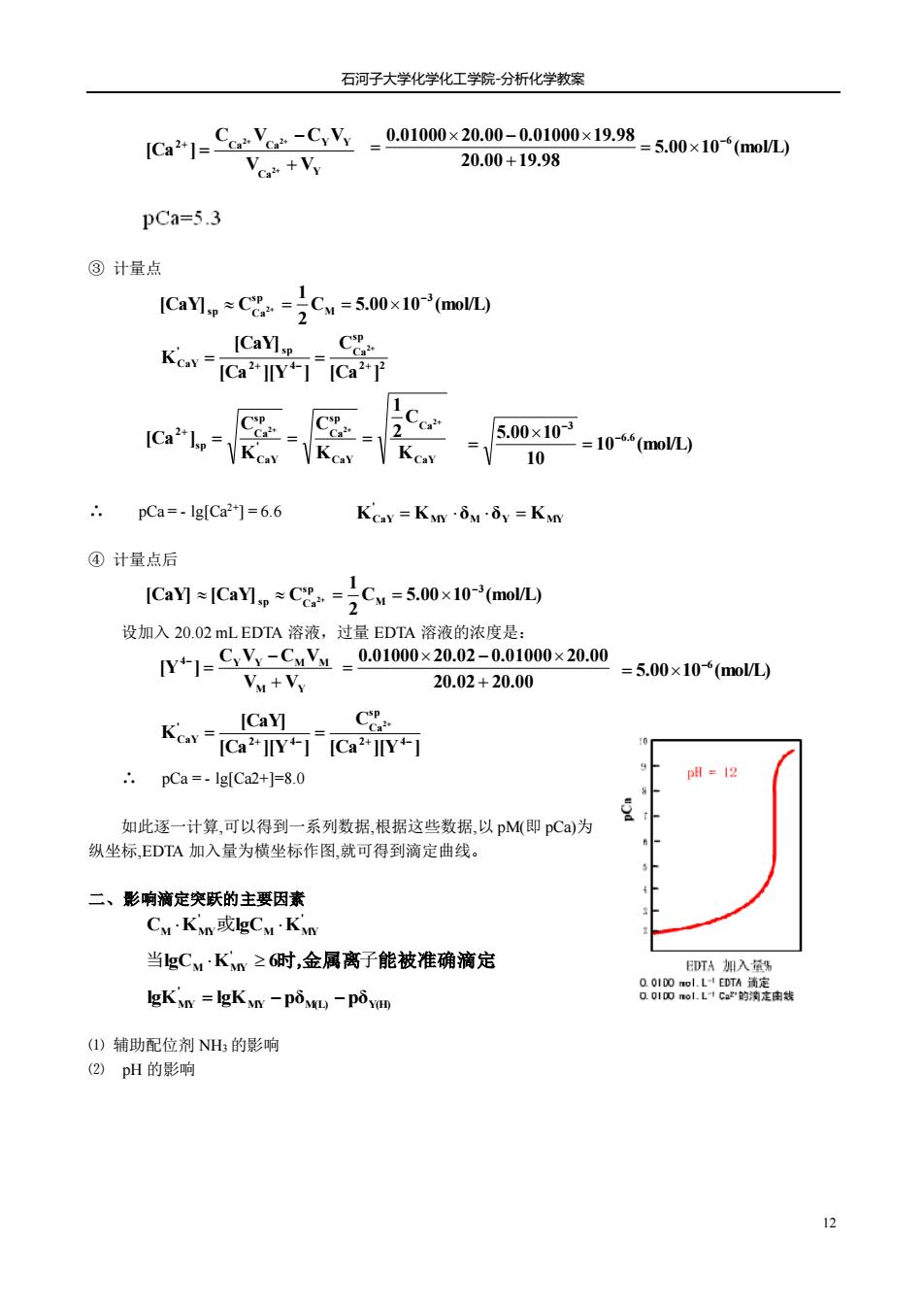
石河子大学化学化工学院分析化学教案 1Ca21=Cayr-CY-00100×2000-0n100x1998-50×10+mon Vo +Vy 20.00+19.98 pCa=5.3 ③计量点 1CaMp*C8=)C4=5.00x10-(mo ICaY] Key-ICaCa ICa"I= =500x10=10*“l 10 pCa=-Ig[Ca2*]=6.6 Kcay=Kn·iui=Kn ④计量点后 ICay]ICaYlC=Cw=5.00x10(moVL) 设加入20.02 mLEDTA溶液,过量EDTA溶液的浓度是: Y+1=CY-CX-0.01000x20.02-0.01000×20.00 Vu+Vy 20.02+20.00 =5.00×10(mol) ICaY] CP Kcav-ICa"T1[Ca2"Y可 .pCa=-Ig[Ca2+]=8.0 如此逐一计算,可以得到一系列数据,根据这些数据,以pM即pCa)为 纵坐标,EDTA加入量为横坐标作图,就可得到滴定曲线。 二、影响滴定突跃的主要因素 CuKn或gCMKy 当gC4·K≥6时,金属离子能被准确滴定 D所A期入男 lgKn=gK-pim-pi画 881四olD满赛唐 ()辅助配位剂NH的影响 (2)pH的影响 石河子大学化学化工学院-分析化学教案 12 ③ 计量点 ∴ pCa = - lg[Ca2+] = 6.6 ④ 计量点后 设加入 20.02 mL EDTA 溶液,过量 EDTA 溶液的浓度是: ∴ pCa = - lg[Ca2+]=8.0 如此逐一计算,可以得到一系列数据,根据这些数据,以 pM(即 pCa)为 纵坐标,EDTA 加入量为横坐标作图,就可得到滴定曲线。 二、影响滴定突跃的主要因素 ⑴ 辅助配位剂 NH3 的影响 ⑵ pH 的影响 Ca Y 2 Ca Ca Y Y V V C V C V [Ca ] 2 2 2 + − = + + + + 5.00 10 (mol/L) 20.00 19.98 0.01000 20.00 0.01000 19.98 −6 = + − = C 5.00 10 (mol/L) 2 1 [CaY] C 3 M sp sp Ca2 − + = = 2 2 sp Ca 2 4 ' sp CaY [Ca ] C [Ca ][Y ] [CaY] K 2 + − + + = = CaY Ca CaY sp Ca ' CaY sp Ca sp 2 K C 2 1 K C K C [Ca ] 2 2 2 + + + = = = + 10 (mol/L) 10 5.00 10 6.6 3 − − = = MY M Y MY ' KCaY = K δ δ = K C 5.00 10 (mol/L) 2 1 [CaY] [CaY] C 3 M s p s p Ca2 − + = = M Y 4 Y Y M M V V C V C V [Y ] + − = − 20.02 20.00 0.01000 20.02 0.01000 20.00 + − = 5.00 10 (mol/L) −6 = [Ca ][Y ] C [Ca ][Y ] [CaY] K 2 4 sp Ca 2 4 ' CaY 2 + − + − + = = ' M MY ' CM KMY或lgC K lgC K 6 . ' 当 M MY 时,金属离子能被准确滴定 MY M(L) Y(H) ' lgKMY = lgK −pδ −pδ