正在加载图片...
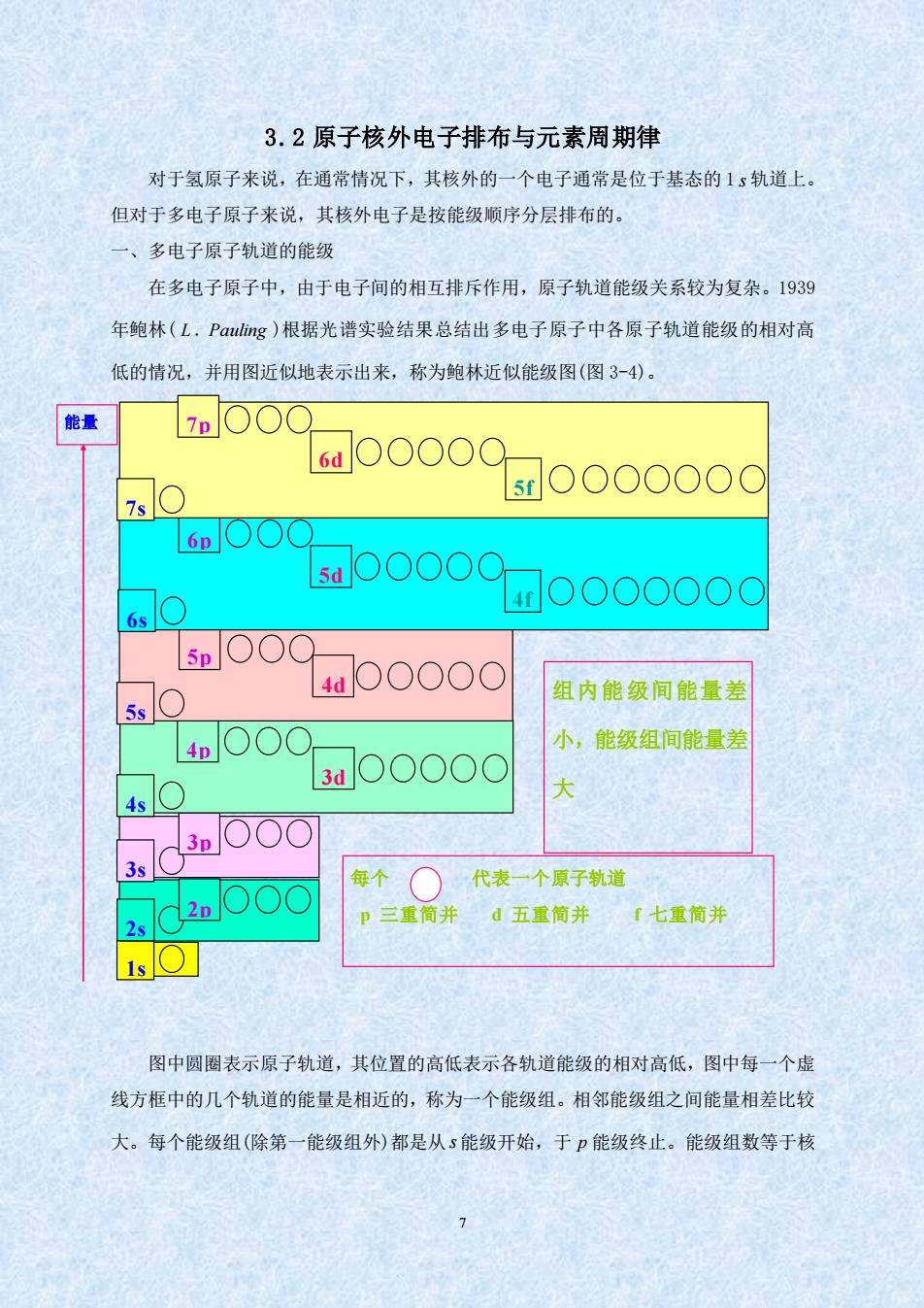
3.2原子核外电子排布与元素周期律 对于氢原子来说,在通常情况下,其核外的一个电子通常是位于基态的1s轨道上。 但对于多电子原子来说,其核外电子是按能级顺序分层排布的。 多电子原子轨道的能级 在多电子原子中,由于电子间的相互排斥作用,原子轨道能级关系较为复杂。1939 年鲍林(L.Pag)根据光谱实验结果总结出多电子原子中各原子轨道能级的相对高 低的情况,并用图近似地表示出来,称为鲍林近似能级图(图3-4), 能量 1000 6dO000 si0O00000 60 sd 000 a0000000 5000 4d000 组内能级间能量差 4nO00 小,能级组间能量差 3a00000 4s1○ 大 300 3s 每个○代表一个原子轨道 p三重简并d五重简并r七重简并 2s 1sO 图中圆圈表示原子轨道,其位置的高低表示各轨道能级的相对高低,图中每一个虚 线方框中的几个轨道的能量是相近的,称为一个能级组。相邻能级组之间能量相差比较 大。每个能级组(除第一能级组外)都是从s能级开始,于能级终止。能级组数等于核7 3.2 原子核外电子排布与元素周期律 对于氢原子来说,在通常情况下,其核外的一个电子通常是位于基态的 1 s 轨道上。 但对于多电子原子来说,其核外电子是按能级顺序分层排布的。 一、多电子原子轨道的能级 在多电子原子中,由于电子间的相互排斥作用,原子轨道能级关系较为复杂。1939 年鲍林( L . Pauling )根据光谱实验结果总结出多电子原子中各原子轨道能级的相对高 低的情况,并用图近似地表示出来,称为鲍林近似能级图(图 3-4)。 图中圆圈表示原子轨道,其位置的高低表示各轨道能级的相对高低,图中每一个虚 线方框中的几个轨道的能量是相近的,称为一个能级组。相邻能级组之间能量相差比较 大。每个能级组(除第一能级组外)都是从 s 能级开始,于 p 能级终止。能级组数等于核 能量 1s 2s 2p 3s 3p 4s 4p 3d 5s 5p 4d 6s 6p 5d 4f 组内能级间能量差 小,能级组间能量差 大 每个 代表一个原子轨道 p 三重简并 d 五重简并 f 七重简并 7s 7p 6d 5f