正在加载图片...
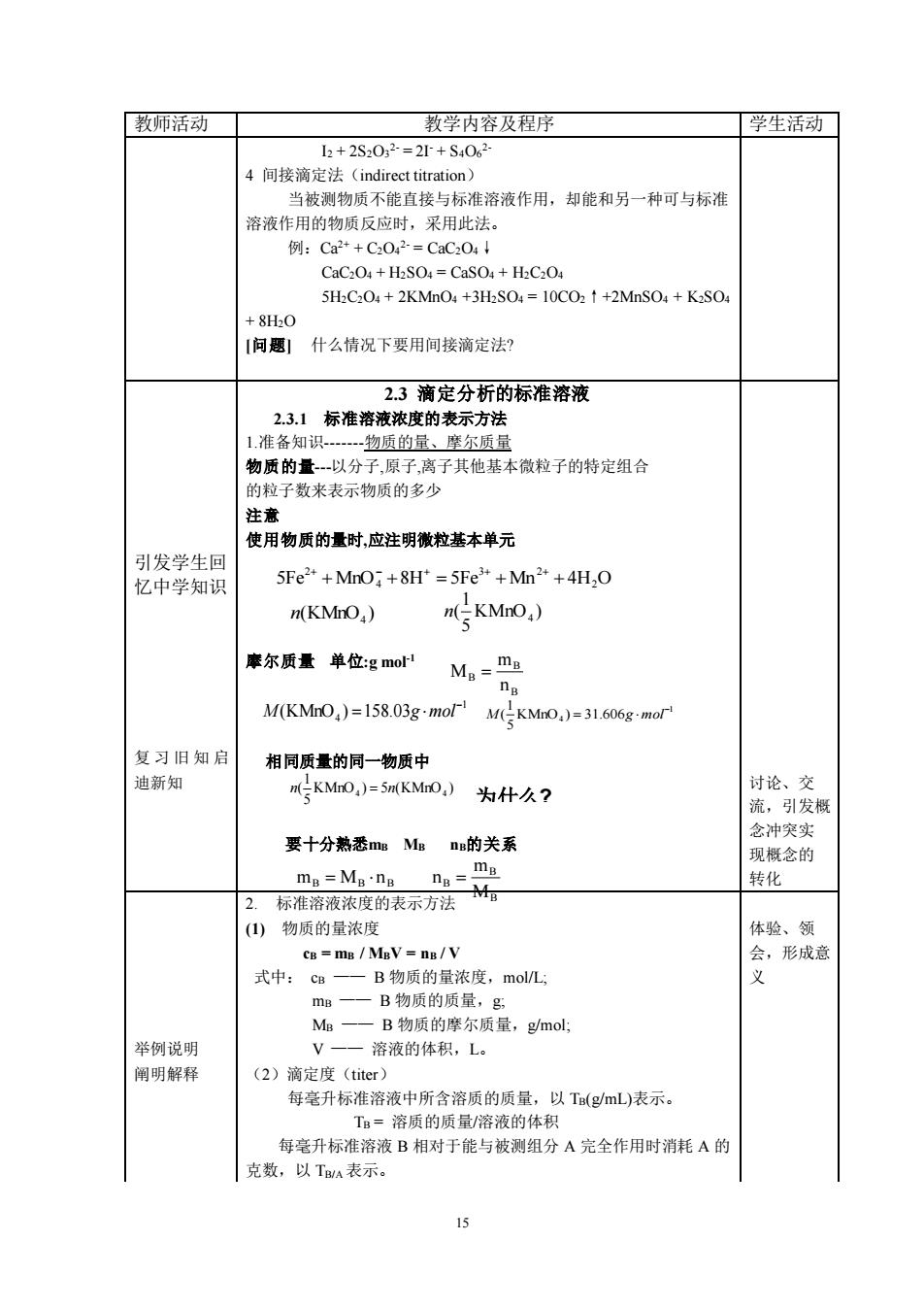
教师活动 教学内容及程序 学生活动 12+2S202=2+S02 间接滴定法( 当被测物质不能直接与标准溶液作用,却能和另一种可与标准 溶液作用的物质反应时,采用此法。 例:Ca2++C202·=CaC204↓ CaC-O4 H2SO+H:C204 5H2C20.+2KMh04+3HS04=10C02+2MnS04+KS0 8H2O [问题!什么情况下要用间接滴定法? 2.3滴定分析的标准溶液 2.3.1 标准溶液浓度的表示方法 1.准备知 -物质的量、尔质量 物质的量以分子,原子,离子其他基本微粒子的特定组合 的粒子数来表示物质的多少 注意 使用物质的量时,应注明徽粒基本单元 引发学生回 忆中学知识 5Fe"+MnO+8H*=5Fe"+Mn?+4H.O n(KMnO,) n(KMn0.) 尔质量单位:gmo n M(KMrO)=158.03g-mol M(KMnO,)-31.606gmo 复习旧知启 相同质量的同一物质中 迪新知 mgKM0,)=5mKM0,)为什久? 讨论、 引发 要十分熟悉me Ma naf的关系 念冲突 现概念的 me =Ma'ng nn=ma 转化 2.标准溶液浓度的表示方法 M 物质的量浓度 体验、领 ca-mB/MaV-nu/V 会,形成 式中:cg一一B物质的量浓度,molL mB一一B物质的质量,g M一一B物质的摩尔质量,gmol: 举例说明 溶液的体积,L。 阐明解 (2)滴定度(iter) 每毫升标准溶液中所含溶质的质量,以T(gmL)表示。 T日=溶质的质量/溶液的体积 每毫升标淮溶液B相对于能与被测组分A完全作用时消耗A的 克数,以T表示。 15 15 教师活动 教学内容及程序 学生活动 I2 + 2S2O3 2- = 2I- + S4O6 2- 4 间接滴定法(indirect titration) 当被测物质不能直接与标准溶液作用,却能和另一种可与标准 溶液作用的物质反应时,采用此法。 例:Ca2+ + C2O4 2- = CaC2O4↓ CaC2O4 + H2SO4 = CaSO4 + H2C2O4 5H2C2O4 + 2KMnO4 +3H2SO4 = 10CO2↑+2MnSO4 + K2SO4 + 8H2O [问题] 什么情况下要用间接滴定法? 2.3 滴定分析的标准溶液 引发学生回 忆中学知识 复习旧知启 迪新知 2.3.1 标准溶液浓度的表示方法 1.准备知识-物质的量、摩尔质量 物质的量-以分子,原子,离子其他基本微粒子的特定组合 的粒子数来表示物质的多少 注意 使用物质的量时,应注明微粒基本单元 摩尔质量 单位:g mol-1 为什要十分熟悉mB MB nB的关系 讨论、交 流,引发概 念冲突实 现概念的 转化 举例说明 阐明解释 2. 标准溶液浓度的表示方法 (1) 物质的量浓度 cB = mB / MBV = nB / V 式中: cB —— B 物质的量浓度,mol/L; mB —— B 物质的质量,g; MB —— B 物质的摩尔质量,g/mol; V —— 溶液的体积,L。 (2)滴定度(titer) 每毫升标准溶液中所含溶质的质量,以 TB(g/mL)表示。 TB = 溶质的质量/溶液的体积 每毫升标准溶液 B 相对于能与被测组分 A 完全作用时消耗 A 的 克数,以 TB/A 表示。 体验、领 会,形成意 义 1 KMnO4 ) 31.606 5 1 ( − M = g mol 1 4 (KMnO ) 158.03 − M = g mol KMnO ) 5 (KMnO ) 5 1 ( 4 4 n = n 相同质量的同一物质中 为什么? KMnO ) 5 1 ( n(KMnO4 ) n 4 5Fe MnO 8H 5Fe Mn 4H2O 3 2 4 2 + + = + + + − + + + B B B n m M = B B B B B B M m m = M n n =