正在加载图片...
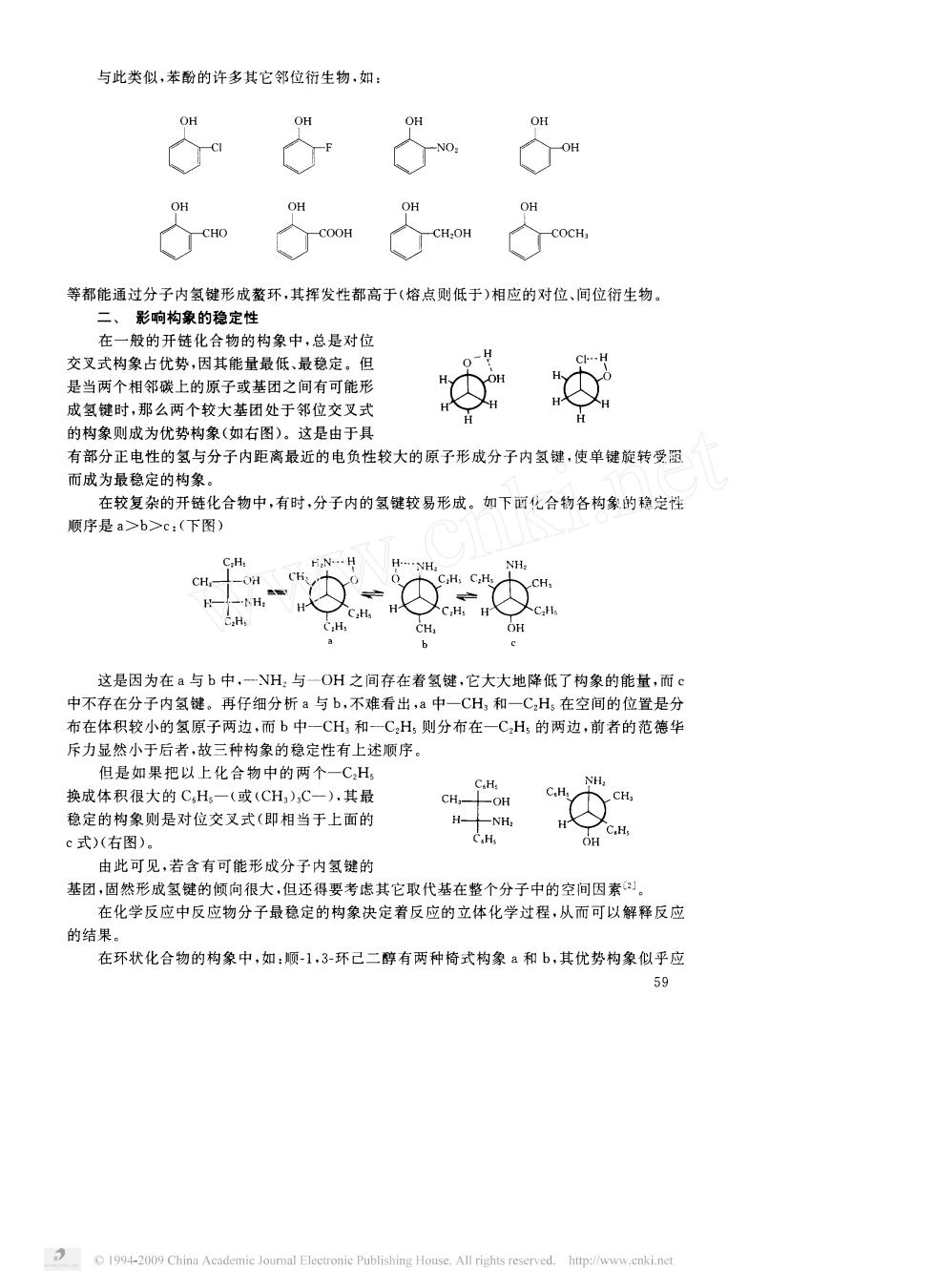
与此类似,苯酚的许多其它邻位衍生物,如: OH .0H 等都能通过分子内氢键形成螯环,其挥发性都高于(熔点则低于)相应的对位、间位衍生物 二、影响构象的稳定性 在一般的开链化合物的构象中,总是对位 交叉式构象占优势,因其能量最低、最稳定。但 是当两个相邻碳上的原子或基团之间有可能形 在 成复缺时,3么质个较大基闭处干邻位空双动 的构象则成为优势构象(如右图)。这是由于具 有部分正电性的氢与分子内距离最近的电负性较大的原子形成分子内氢键,使单键旋转受器 而成为最稳定的构象 在较复杂的开链化合物中,有时,分子内的氢键较易形成。如下面化合物各构象的稳定性 顺序是a>b>c:(下图) 这是因为在a与b中,一NH:与一OH之间存在着氢键,它大大地降低了构象的能量,而。 中不存在分子内氢键。再仔细分析a与b,不难看出,a中一CH,和一C,H,在空间的位置是分 布在体积较小的氢原子两边,而b中CH,和一C,H,则分布在一C,H的两边,前者的范德华 斥力显然小于后者,故三种构象的稳定性有上述序 但是如果把以 上化合物中的两个C,H 换成体积很大的C,H一(或(CH,),C-),其最 稳定的构象则是对位交义式(即相当于上面的 c式)(右图)。 由此可见,若含有可能形成分子内氢键的 基团,固然形成氢健的倾向很大,但还得要考虑其它取代基在整个分子中的空间因素, 在化学反应中反应物分子最稳定的构象决定者反应的立体化学过程,从而可以解释反应 的结 在环状化合物的构象中,如:顺-1.3环已二醇有两种椅式构象a和b,其优势构象似乎应 59 0 China Academic Jouma Electronie Publishing Hous.All rights reserved.http://www.enkinct 与此类似 , 苯酚 的许多其 它邻 位衍 生物 , 如 分 , 分 · 断 沙 · 分 二 护 。。· 沙一 沙 。二 等都能通过分子 内氢键形 成 鳌 环 , 其挥发性都高 于 熔 点则低 于 相 应 的对 位 、 间位衍 生物 。 二 、 影响构象的稳定性 在 一般 的开链 化合物 的构 象 中 , 总是 对 位 占人丫 刀 、 义日 交叉 式构象 占优 势 未人丫 , 因其 能量最低 、 最 稳 定 。 但 是 当两个相邻 碳上 的原子 或基 团之 间有可能形 成氢键 时 , 那 么两个较大基 团 处于 邻位交 叉 式 的构象则成为优势构象 如右 图 。 这是 由于具 有部分正 电性 的氢与分子 内距离最近 的 电负性 较大 的原 子形 成分 子 内氢键 , 使单 键 旋 转 受 阻 而成 为最稳定的构象 。 在较复杂 的开链化合物中 , 有 时 , 分子 内的氢键较 易形 成 。 如下 面化合 物各构象 的稳 定性 顺序是 下 图 导 今一砰 毕一 明 一十 一 丫卜 。 。 刊丫 ’ 过乍卜 一卜 戈必 , 洲 狡 该 产 狡笋 , , , 人 , , 一 上 少 ℃ 七 这是 因为在 与 中 , 一 与一 之 间存在着 氢键 , 它大大地 降低 了构象的能量 , 而 。 中不存在分子 内氢键 。 再仔 细分析 与 , 不难看 出 , 中一 。 和 一 。 在 空 间的位置是分 布在体积较 小的氢原子 两 边 , 而 中一 和一 则分布在一 的两 边 , 前者 的范德华 斥力显 然 小于后者 , 故三种构象 的稳 定性有上述顺序 。 润践“, 蕊人丫夕、、 但 是 如 果 把 以 上 化 合 物 中 的 两 个一 换成 体 积 很大 的 一 或 。 一 , 其 最 稳 定 的构 象则 是 对 位交 叉 式 即相 当于 上 面 的 式 右图 。 由此 可见 , 若 含 有 可 能 形 成分 子 内氢 键 的 · 十月一 , 基 团 , 固然形成 氢键 的倾 向很大 , 但还 得要 考虑 其 它取 代基 在整个分子 中的空 间 因 素川 。 在化学 反 应 中反 应物分子最 稳 定的构象决 定着反 应 的立 体化学 过 程 , 从而 可 以解释 反应 的结果 。 在 环状化合 物 的构 象 中 , 如 顺 一 , 一 环 己 二 醇 有两 种椅 式构象 和 , 其优 势构象似乎应