
试卷代号:2035 座位号■■ 中央广播电视大学2008一2009学年度第二学期“开放专科”期末考试(半开卷) 农科基础化学试题 2009年7月 题号 二 三 四 五 六 七 八 总 分 分数 无机分析化学部分 得分 评卷人 一、单项选择题(每小题2分,共10分) 1.已知下列气体反应(在一定温度下) 反应I:A=B 平衡常数为K) 反应I:B十C一D 平衡常数为K2) 下列哪种表示为A十C一D的K()。 A.K1)/K2 B.KR2/KPL) C.Kr)·Kp2 D.[Kw·K2]2 2.下列哪一条不是基准物质所应具备的条件()。 A.与化学式相符的物质组成 B.不应含有结晶水 C.纯度应达99.9%以上 D.在通常条件应具有相当的稳定性 3.用加热法驱除水分以测定CaS0,·2H,0中结晶水的含量,称取试样0.2000g,已知 天平称量误差为士0.1mg。试问分析结果应以几位有效数字报出?() A.一位 B.二位 C.三位 D.四位 4.用SO?使Ba+形成BaSO4沉淀时,加入适量过量的SO,可以使Ba+离子沉淀更 完全,这是利用何种效应( ) A.盐效应 B.酸效应 C.络合效应 D.同离子效应 177
试卷代号:2035 座位号口二」 中央广播电视大学2008-2009学年度第二学期“开放专科”期末考试(半开卷) 农科基础化学 试题 2009年 7月 题 号 四 五 六 七 八 总 分 分 数 无机分析化学部分 得 分 评卷人 一、单项选择题(每小题 2分,共 10分) 1.已知下列气体反应(在一定温度下) 反应 I:A -B 平衡常数为 Kp(j) 反应 I:B十C - D 平衡常数为 KP(2) 下列哪种表示为 A+C v二=D的 KP )。 A. Kp(j) /KP(z) B. KP(z)/Kp(j) C. Kp(j)·KP(z) D. [KP(j)·KP(2)〕2 2.下列哪一条不是基准物质所应具备的条件( )。 A.与化学式相符的物质组成 B.不应含有结晶水 C.纯度应达 99. 9%以上 D.在通常条件应具有相当的稳定性 , 、_二 、,_=’t。。人 ,_,、.、,,,二 _ _。 1,__ .,。_。 . ,*_ _,_ _、 _ _ . “·用加热法驱除水分以测定CaS04·言H2O中结晶水的含量,称取试样。. 2000g,已知 天平称量误差为士0. lmg。试问分析结果应以几位有效数字报出?( ) A.一位 B.二位 C.三位 D.四位 4.用 SO专一使 Baz+形成 BaSO;沉淀时,加人适量过量的 SO芝一,可以使 Baz+离子沉淀更 完全,这是利用何种效应( )。 A.盐效应. B.酸效应 C.络合效应 D.同离子效应 177

5.属于紫外可见分光光度计的波长范围是多少nm()。 A.200~1000 B.420~700 C.360~800 D.400~800 得分 评卷人 二、是非题(每小题2分,共10分) 1.若改变影响化学平衡的一个条件,使平衡向正反应方向移动,一定能提高某种反应物的 转化率。 () 2.滴定终点一定和等量点是吻合的。 () 3.相同浓度的NaOH溶液和NH,溶液中OH-浓度相同。 () 4.因为Ag2CrO4的Kp(2.0X10-12)小于AgCl的Kp(1.6X10-10),所以Ag2CrO4必定 比AgCI更难溶于水。 () 5.在分光光度分析中,吸光度愈大,测量的误差愈小。 () 得 分 评卷人 三、计算题(每小题8分,共24分) 1.150 mL NaHCO3注射液中含有7.50 g NaHCO3,计算此注射液的质量浓度和物质的量 浓度。(M(NaHCO3)=84.0g·mol-1)(8分) 2.计算0.45mol·LNH,C1溶液的pH值。(已知Kb(NH,)=1.8X10-5)(8分) 3.计算298K时Fe3+/Fe2+,c(Fe3+)=0.1mol·L-1,c(Fe2+)=0.5mol·L1电对的电 极电势。(已知p++=0.771V)(8分) 得 分 评卷人 四、(6分} 命名[Co(NH)C1]+配离子,并指出中心原子、配体、配位原子和配位数。 178
5.属于紫外可见分光光度计的波长范围是多少 nm( )。 A. 200.1000 B. 420一700 C. 360- 800 D. 400一 800 得 分 评卷人 二、是非题(每小题 2分 .共 10分 ) 1.若改变影响化学平衡的一个条件,使平衡向正反应方向移动,一定能提高某种反应物的 转化率。 ( ) 2.滴定终点一定和等量点是吻合 的。 ( ) 3.相 同浓度的 NaOH溶液和 NH,溶液中 OH一浓度相同。 ( ) 4.因为Age CrO‘的K,p (2. 0 X 10-12)小于AgCl的K,(1.6X10-10),所以Age CrO;必定 比AgCl更难溶于水。 · ( ) 5.在分光光度分析中,吸光度愈大,测量的误差愈小。 ( ) 得 分 评卷人 三、计算题(每小题 8分。共 24分 ) 1. 150mL NaHCO。注射液中含有7. 50g NaHCO,,计算此注射液的质量浓度和物质的量 浓度。(M(NaHCO,) =84. Og·mol-') (8分) 2.计算 0. 45mol " L-'NH,CI溶液的 pH值。(已知 K6(NH,)二1.8X10-5) (8分) 3.计算 298K时 Fe" /Fe2+,c(Fe3+)=0. 1 mol " L-',c(Fe2+)=0. 5 mol " L-‘电对的电 极电势。(已知甲IPaFe3+/Fe2+ =0. 771V) (8分) 得 分 评卷人 四、(6分} 命名〔Co (N H, ), Cl l2+配离子,并指出中心原子、配体、配位原子和配位数。 178
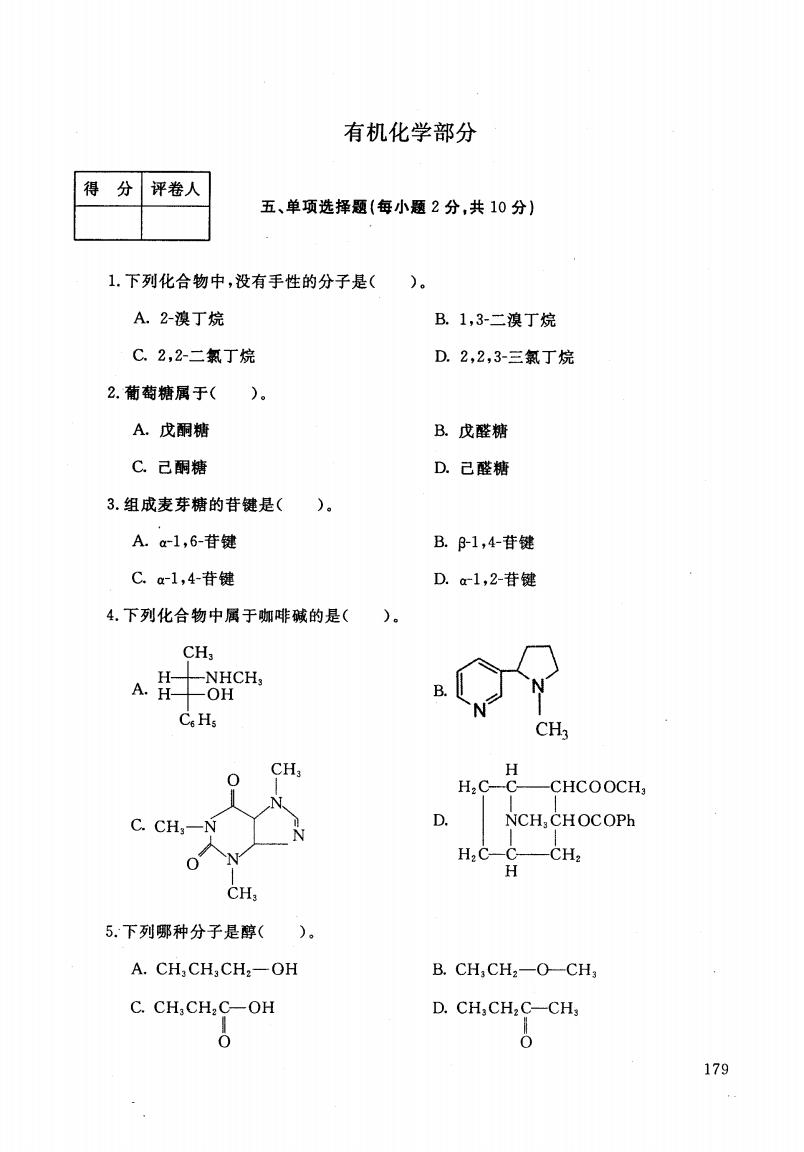
有机化学部分 得分 评卷人 五、单项选择题(每小题2分,共10分) 1.下列化合物中,没有手性的分子是( )。 A.2-溴丁烷 B.1,3-二溴丁烷 C.2,2-二氯丁烷 D.2,2,3-三氯丁烷 2.葡萄糖属于( )。 A.戊酮糖 B.戊醛糖 C.己酮糖 D.己醛糖 3.组成麦芽糖的苷键是()。 A.a-1,6-苷键 B.B-1,4-苷键 C.a-1,4-苷键 D.c1,2-苷键 4.下列化合物中属于咖啡碱的是()。 CH, H -NHCH, A. OH B. CoHs CH 0 CH; H2C-C CHCOOCH C.CH D. NCH,CHOCOPh H2C- C H CH: 5.下列哪种分子是醇( )。 A.CH,CH,CH2-OH B.CHCH2一O-CH C.CH,CH2C-OH D.CH,CH2C-CH, 0 17
有机化学部分 得 分 评卷人 五、单项选择题(每小题 2分,共 10分) 1.下列化合物中,没有手性的分子是( A. 2-澳丁烷 C. 2,2一二氯丁烷 B. 1,3一二澳丁烷 D. 2,2,3一三氯丁烷 2一葡萄糖属于( A.戊酮糖 C.己酮糖 B.戊醛糖 D.己醛糖 3.组成麦芽糖 的昔键是 ( A. a-1,6-昔键 C. a-1, 4-昔键 B. P-1,4-昔键 D. a-1,2-昔键 、、、/ H - “、I C 今 N 4.下列化合物中属于咖啡碱的是( )。 CH, A.。牛 C, H NO,HCH, CH H HZC- C CHCOOCH C. CH D. NCH, CH OC OPh HZ C- ()一-一CH, H CH 5:下列哪种分子是醇( A. CH, CH, CH:一 OH B. CH, CHZ- O- CH C. CH,CHZC- OH }} D. CH3 CHZ C-CH } O 179
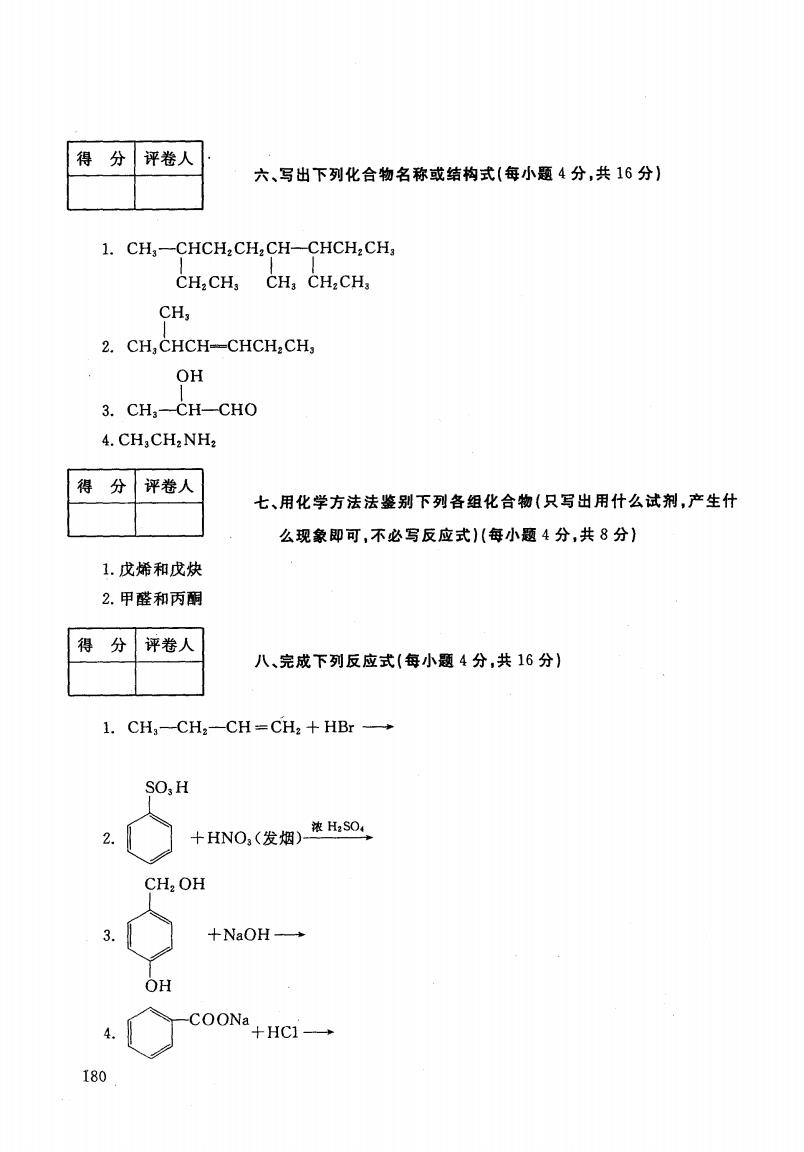
得分 评卷人 六、写出下列化合物名称或结构式(每小题4分,共16分) 1.CH,-CHCH,CH2 CH-CHCH:CH, CHCH,CH,CH.CH, CH, 2.CH,CHCH--CHCH:CH, OH 3.CHCH—CHO 4.CH:CH2NH2 得分 评卷人 七、用化学方法法鉴别下列各组化合物(只写出用什么试剂,产生什 么现象即可,不必写反应式)(每小题4分,共8分)】 1.戌烯和戊炔 2.甲醛和丙酮 得分 评卷人 八、完成下列反应式(每小题4分,共16分) 1.CH;-CH2-CH=CH2 +HBr- SO:H 2. +HNO,(发烟) 浓HSO4 CH,OH 3. +NaOH- OH 4. C0ONa+HC1一 180
得 分 评卷人 六、写出下列化合物名称或结构式(每小题 4分,共 16分) , ·CH,一甲 C H H C ZC H H Z C, HZ甲 C H H-, C C H H C ZC H H Z CH, CH, } 2. CH,CHCH-CHCHZCH, OH 1 3. CH3-CH- CHO 4. CH,CHZNHZ 得 分 评卷人 七、用化学方法法鉴别下列各组化合物 (只写出用什么试剂 ,产生什 么现象即可.不必写反应式 )(每小题 4分.共 8分) 1.戊烯和戊炔 2.甲醛和丙酮 得 分 评卷人 11、完成下列反应式(每小题 4分.共 16分 ) 1. CH3-CHZ-CH =CH:十HBr一 S03 H 2. CHZ O 一 H ’卜 3.中 OH 一 180 4.今 COONa+HC‘一

试卷代号:2035 中央广播电视大学2008一2009学年度第二学期“开放专科”期末考试(半开卷) 农科基础化学试题答案及评分标准 (供参考) 2009年7月 无机分析化学部分 一、单项选择题(每小题2分,共10分)】 1.C 2.B 3.C 4.D 5.A 二、是非题(每小题2分,共10分】 1.错 2.错 3.错 4.错 5.错 三、计算题(每小题8分,共24分】 1.(8分) 因为溶液的体积V=150mL=0.150L (1分) NaHCO3质量m=7.50g (1分) @(NaHC0,)=75=50.0g·L 0.150L (3分) p(NaHC0)=50.0=0.595(mol·L-1) c(NaHCO,)-M(NaHCO,)84.0 (3分) 2.(8分) Kw _1.0×10-14 K.NH时)=KNH-.8X10=5.6X10-0 (2分) .0.45 ”c(NH时)/K,=5.6X10-500,可采用最简式: (1分) .[H+]=√K.×c(NH万=√5.6×10-0×0.45=1.6×10-5 (3分) pH=-lg[H+]=-lg(1.6×10-3)=4.80 (2分) 3.(8分) 已知1e+R2+=0.771V Fes++e=Fe2+ (2分) 0.05921g(Fe+) c(Fe2+) (2分) -0.71+0.05921lg8g0.73v (4分) 181
试卷代号:2035 中央广播电视大学2008-2009学年度第二学期“开放专科”期末考试(半开卷) 农科基础化学 试题答案及评分标准 (供参考) 2009年7月 无机分析化学部分 一、单项选择题(每小题 2分,共 10分) 1. C 2. B 3. C 4. D 二、是非题(每小题 2分,共 10分) 1.错 2.错 3.错 4.错 三、计算题(每小题 8分,共 24分) 1. (8分) 因为溶液的体积 V= l50mL=0. 150L NaHCO,质量 m=7. 50g 5. A 5.错 p(NaHCO,)= 7. 50g= 0. 150L 50. Og·L-1 > 500,可采用最简式 : 5.6X10一iV‘----7J/一,,;~ .、。 . :. [H+〕二-,/K, X c(NH才)二V5. 6 X 10一‘。X0. 45二1.6X10一s pH=一1gEH+〕=一lg(1. 6 X 10一”)=4. 80 3.(8分) 已知,Fe ,/Fe 十=0. 771V Fe' +e=Fe2+ (2分) (I分) (3分) (2分) ,=T'+O. 05921g c(Fe+) c (Fe2+) (2分) (2分) 。 。,,,_ _尸。。,, 0.1 _ ,,,、了、 = U. III一 U. USyzllg - U o d U. 7,51 V ) (4分) 181

四、(6分) 氯·五氨合钴(Ⅲ)配离子(2分)中心原子Co+(1分)配体C1、NH,(1分)配位原子Cl、 N(1分)配位数6(1分) 有机化学部分 五、单项选择题(每小题2分,共10分)】 1.C 2.D 3.D 4.C 5.A 六、写出下列化合物名称或结构式(每小题4分,共16分) 1.4,7-二甲基-3-乙基壬烷 2.2-甲基-3-己烯 3.2-羟基丙醛 4.乙胺 七、用化学方法法鉴别下列各组化合物(只写出用什么试剂,产生什么现象即可,不必写反应 式)(每小题4分,共8分) 1.戊婚) 硝酸银的氨溶液 无沉淀 '戊炔了(或氯化亚铜的氨溶液)白色(或红棕色)沉淀 丙酮)1,+NaOH黄色沉淀 2. 甲醛, 无沉淀 八、完成下列反应式(每小题4分,共16分) 1.CH,-CH2-CH-CH, Br SO,H 2. CH2 OH 3. OH 182
四、(6分 ) 氯·五氨合钻(m)配离子(2分)中心原子Co" (1分)配体C1-,NH3(1分)配位原子Cl, N (1分)配位数 6(1分) 有机化学部分 五、单项选择题(每小题 2分,共 10分》 1.C . 2. D 3. D 4. C 5. A 六、写出下列化合物名称或结构式(每小题 4分,共 16分) 1.4,7一二甲基一3一乙基壬烷 2.2一甲基一3一己烯 3.2一经基丙醛 4.乙胺 七、用化学方法法鉴别下列各组化合物f只写出用什么试剂,产生什么现象即可,不必写反应 式)(每小题 4分 .共 8分) Mft1}t N4f1l 硝酸银的氮溶液 (或抓化亚铜的氨溶液) 无沉淀 白色(或红棕色)沉淀 IZ+NaOH 黄色沉淀 无沉淀 八 、完成下列反应式(每小题 4分 .共 16分》 1. CH,-CH,-CH-CH r ! B NO, CH, OH ,/}k--000H 4. 182