
试卷代号:2123 座位口 中央广播电视大学2009一2010学年度第一学期“开放专科”期末考试(半开卷) 医用基础化学 试题 2010年1月 题 号 一 二 三 四 五 六 总分 分 数 无机及分析化学部分 :分 评卷人 一、选择题(每小题2分,共10分) 1.碳酸钙的分解反应:CaCO3=CaO(s)+CO2(g),其标准平衡常数表达式为( A.K-([Ca([CO:) ([CaCO,]/c) B.K=Pco/p C.KCo D.K=[C02]/p ([CaCO:]/c) 2.下列沉淀可溶于NH,CI溶液的是( A.CuS B.AgCl C.Mg(OH) D.BaSO. 3.以sp2杂化轨道成键的BF,分子的空间构型是( ) A.三角锥形 B.平面三角形 C.直线性 D.四面体型 4.下列哪一条不是一级标准物质(基准物质)所应具备的条件( ) A.与化学式相符的物质组成 B.不应含有结晶水 C.纯度应达99.9% D.在通常条件下应具有相当的稳定性 664
试卷代号:2123 座位号【二口 中央广播电视大学2009-2010学年度第一学期“开放专科”期末考试(半开卷) 医用基础化学 试题 2010年 1月 题 号 四 五 六 总 分 分 数 无机及分析化学部分 得 分 评卷人 一、选择题(每小题 2分,共 10分) 1.碳酸钙的分解反应:CaC03 =CaO(s)-}-COz (g),其标准平衡常数表达式为( A. Ke二 ([Ca0]/ce )(仁COz ]/1}e ) ( [CaCO, ]/ce ) B. Ke二hcoZ /pe C. K。二 (仁Ca0]/ca) ([pco. ]/pe ) ( [CaC03〕/。。) D. Ke=[COz ]/pe 2.下列沉淀可溶于NH,CI溶液的是( CuS Mg(OH)z ) B. AgCI D. BaSO A. C. 3.以sp,杂化轨道成键的BF3分子的空间构型是( A.三角锥形 C.直线性 B.平面三角形 D。四面体型 4,下列哪一条不是一级标准物质(基准物质)所应具备的条件( A.与化学式相符的物质组成 C.纯度应达 99. 9 B.不应含有结晶水 D.在通常条件下应具有相当的稳定性 664

5.在定量分析中,减小偶然误差的方法是( A.空白实验 B.对照试验 C.校正仪器 D.增加平行测定次数 得分 评卷人 二、问答题(每题5分,共10分) 1.将Fe十Cu+=Fe2++Cu氧化还原反应设计成原电池,分别写出他们的反应和电池符 号。(5分) 2.命名K,[Pt(SCN)6]配合物,并指出中心原子、配体、配位原子和配位数。(5分) 得 分 评卷人 三、计算题(30分) 1.正常人血浆中每100mL含Na+0.356g,求其物质的量浓度(用mol·L1表示)。 (M(Na+)=23.0g/mol)(6分) 2.计算10.0g·L1KC1溶液在37℃时的渗透压。(Mx=74.6g·mol-1)(6分) 3.计算0.45mol·L-1NH,C1溶液的pH值。(已知K.(NH3)=1.8×105)(6分) 4.0.20mol·L1NaH2PO.溶液10.0mL与0.25mol·L1Na2HPO4溶液20.0mL积 混合,求混合溶液的pH值。(已知pK.(HzPO)=7.21)(6分) 5.计算298K时:Cr2O号/Cr3+,c(Cr2O)=0.2mol·L-1,c(Cr3+)=0.3mol·L1, c(H+)=3mol·L电对的电极电势。(已知p呢,心+=1.232V)(6分) 有机化学部分 得分 评卷人 四、给下列化合物命名或写出结构式(每小题4分,共20分) 1.OH 2.叔丁胺 665
5.在定量分析中,减小偶然误差的方法是( A.空 白实验 C.校正仪器 B.对照试验 D.增加平行测定次数 得 分 评卷人 二、问答题 (每题 5分.共 10分 ) 1.将 Fe}-Cu2+ =Fez十+Cu氧化还原反应设计成原电池,分别写出他们的反应和电池符 号 。(5分) 2.命名 KZ [Pt(SCN)6〕配合物,并指出中心原子、配体、配位原子和配位数。(5分) 得 分 评卷人 三、计算题(30分) 1.正常人血浆中每 100mL含 Na+ 0, 356g,求其物质的量浓度 (用 mol " L-‘表示)。 (M(Na+)=23. Og/mol) (6分) 2.计算 10. 0g " L-1 KCl溶液在 3 7 0C时的渗透压。(MK}, =74, 6g " mol-' ) (6分) 3.计算 0. 45mo1 " L--' NH4C1溶液的 pH值。(已知 I{b(NH3)=1. 8X 10-5)(6分) 4, 0. 20mo1·L-' NaHz PO,溶液 10. OmL与 0, 25mo1·L-' Nat HPO;溶液 20. OmL积 混合,求混合溶液的 pH值。(已知 pK"(HZPOa)=7.21)(6分) 5.计算 298K时:Cr2 O弓一/Cr3+,c(CrZO专一)= 0. 2 mol·L-' ,c(Cr'+)= 0, 3 mol·L ’, c<H+)=3rnol " L-‘电对的电极电势。(已知}psc}2 0琴一/c}3十=1, 232V)(6分) 有机化学部分 得 分 评卷人 四、给下列化合物命名或写出结构式(每小题 4分 ,共 20分) L分 2.叔丁胺 OH 665

OH 3. CH-COOH 4.3-甲基环己酮 5.对-硝基苯乙酮 得分 评卷人 五、完成下列反应式,写出主要产物(每题4分,共20分) CH2 +HI→ CH, 2.CH,C-CH,CH,_浓as0, △ OH 3.CH,-C-COOH NH,-NH -NO;- NOz 4.CH,-CH-CH2-COOH— 加热 OH 5.CH -NH2+HCI→ 得分 评卷人 六、问答题(共10分) 1.分子式C6H1的化合物A,加人Br2的CCL,溶液,溴的颜色褪去生成B,A催化氢化时 吸收1摩尔的H2生成C,C在紫外光的作用下与CL2反应生成一种一氯代产物D,试推测A、 B、C、D的结构。(4分) 2.解释对映体的概念。(3分) 3.解释变旋光现象的含义。(3分) 666
OH 3.导CH-COON 3一甲基环己酮 对一硝基苯 乙酮 得 分 评卷人 五、完成下列反应式 ,写出主要产物(每题 4分,共 20分) CH 1.丫 +H‘一 CH CH CH3 } C--CHZCH ! OH 浓 x}so, - 一-一一一-一 一一一-一一一- △ - C- COON 十 NHZ- NH母 NO 4, CH3-CH-CHZ-000H i NOZ 加热 。 O OH 5. CH,e{卜 NHz.+HCl 得 分 评卷人 六、问答题 (共 l0分) 1.分子式C6 H,。的化合物 A,加人 Br2的GCl4溶液,澳的颜色褪去生成 B, A催化氢化时 吸收 1摩尔的 H:生成 C,C在紫外光的作用下与 Cl:反应生成一种一氯代产物 D,试推测 A, B,C,D的结构。(4分) 2.解释对映体的概念。<3分) 3.解释变旋光现象的含义。(3分) 666

试卷代号:2123 中央广播电视大学2009一2010学年度第一学期“开放专科”期末考试(半开卷) 医用基础化学 试题答案及评分标准 (供参考) 2010年1月 无机及分析化学部分 一、选择题(每小题2分,共10分) 1.B 2.C 3.B 4.B 5.D 二、问答题(每题5分,共10分) 1.(5分) 正极(还原反应)Cu++2e=Cu(1分) 负极(氧化反应)Fe一2e=Fe2+(1分) 电池符号:(-)Fe|Fe2+(c1)‖Cu+(c2)Cu(+)(3分) 2.(5分) 六(硫氰酸根)合铂(V)酸钾(1分),中心原子Pt+(1分),配体SCN(1分),配位原子S (1分),配位数6(1分) 三、计算题(30分)】 1.(6分) 解:因为 m=0.356=0.0155(mol) n(Na+)=MNa523.0 (2分) V-80h=0.1oL1分) c(Na+)=uNa*)_0.015m0=0.155mol.L1(3分) 0.100L 2.(6分) 解:,KCl溶液的浓度c=p/M(1分) ÷c=76=0.134(molL)1分) KCI是A一B型强电解质,据渗透压公式:(1分) 667
试卷代号:2123 中央广播电视大学2009-2010学年度第一学期“开放专科”期末考试(半开卷) 医用基础化学 试题答案及评分标准 (供参考) 2010年 1月 无机及分析化学部分 一、选择题(每小题 2分.共 10分) 1. B 2. C 3. B 4. B 5. D 二、问答题 (每题 5分,共 10分 ) 1. (5分) 正极(还原反应)CuZ+-}-2e=Cu (1分 ) 负极(氧化反应)Fe-2e=Fe2+ (1分) 电池符号:(一)Fe } Fe2+ (c, )}CuZ+(c2)}Cu(-I-) (3分) 2. (5分) 六(硫氰酸根)合铂(}r)酸钾(1分),中心原子 Pt"+ (1分),配体 SCN- (1分),配位原子 S (1分),配位数 6(1分) 三、计算题 (30分) 1. (6分) 解:因为 n(Na+)=M ( Na+) 0. 356 23. 0 =0.0155(mol) (2分) 100mL V = 丁花丁二二厂一一丁二几广= u lUUUmI/ 1, 100L (1分) ,、,、、 n(Na+t) 0. 0155mo1 d iva }= 一一,丁厂- .= 钾一二-:-万丁下- = u V U. lUU L 155mo1·L-' ( 3分) 2. (6分) 解:’: KCl溶液的浓度。=洲M (1分) c=黑 1任 。0 一。.134 (mol.L-' ) (1分) KCI是 A-}3型强电解质 ,据渗透压公式: <1分) 667

Ⅱ=icRT=2×0.314×8.314×(273+37)=691(kPa)(3分) 3.(6分) 解:k(N)-KD8x8-5.6X10”1分 0.45 :cNH)/K,5.6X10-西》500,可采用最简式:(1分) .[H+]=√K.×c(NH)=5.6X100×0.45=1.6×105(3分) pH=-lg[H*]=-1g(1.6×10-5)=4.80(1分) 4.(6分) 解:此混合溶液是H2PO,一HPO缓冲溶液,已知pK.(H2PO)=7.21(1分) 混合液H2PO:和HPO?浓度分别为: (H,P0i)889品。-0.067 ol1)分 (Po)-8028¥88-0167moL1分) pH=pK,+a号}=7.21+1g88-721+040=7613分) 5.(6分) 解:已知p呢,时心3+=1.232V Cr2O+14H++6e=2Cr3++7H2O (2分) p=9+0052gC02C2r1H c2(Cr3+) (2分) -1.232+05031g48x"-1.301w (2分) 有机化学部分 四、给下列化合物命名或写出结构式(每小题4分,共20分) 1.环己醇 NH2 2.CH3-C-CH, CH 3.a羟基苯乙酸 668
I二icRT=2X0.314X8.314X(273-X37)=691(kPa) (3分) 解 <6分) :Ke<NH;)一瓦K6(KNwH3)一1l. . 0 8 X 110-1'"一5.6X,。一<1分) c(NH才)/K8“ 0. 45 5. 6火 10一io;500,可采用最简式: (1分) [H+]=了K, X c<NH;) =}/5. 6 X 10一‘0X0.45=1.6X10-"5 (3分) pH=一lg[H}〕二一1g(1. 6 X 10_5)二4. 80 (1分) 4. (6分) 解:此混合溶液是 HZP04 - HPO三一缓冲溶液,已知 pKe(HZPOa )=7.21 (1分) 混合液 HZ P04和 HPO是一浓度分别为: c( HZ P04)= 0. 2OX 10 20. 0 -I-10. 0 二0. 067mo1 。(HZ PO三- 0. 25 X 20. 0 20. 0一卜10. 0 = 0. 167mo1 ·L-' (1分) ·L-' < 1分) c( HPO若一) ,。,,, 0. 167 P且= P八。十 1g号 irr nn-}= /.Zl卞 1g n一 nc"7 〔气n 2rv 4夕 v. vv } =7. 21-0, 40=7. 61 (3分) 5. <6分) 解:已知喊}ZO;-ic*'+ =1, 232V Cr2 O季一+14H}-}6e=2Cr3+-}-7H20 (2分) 了、 一、 夕 。.0. 0592. p= 甲“十一一c U 一 lg c(Cr20李一)C14 cz (Cra+ H+ (2分 ) 1. 232+0. 0 U59210.2X3" 0. 3 Z 301(V) <2分 ) 有机化学部分 四、给下列化合物命名或写出结构式(每小题 4分 。共 20分) 1.环 己醇 NHZ 2. CH,一 (',- CH } CH 3. a-经基苯 乙酸 668
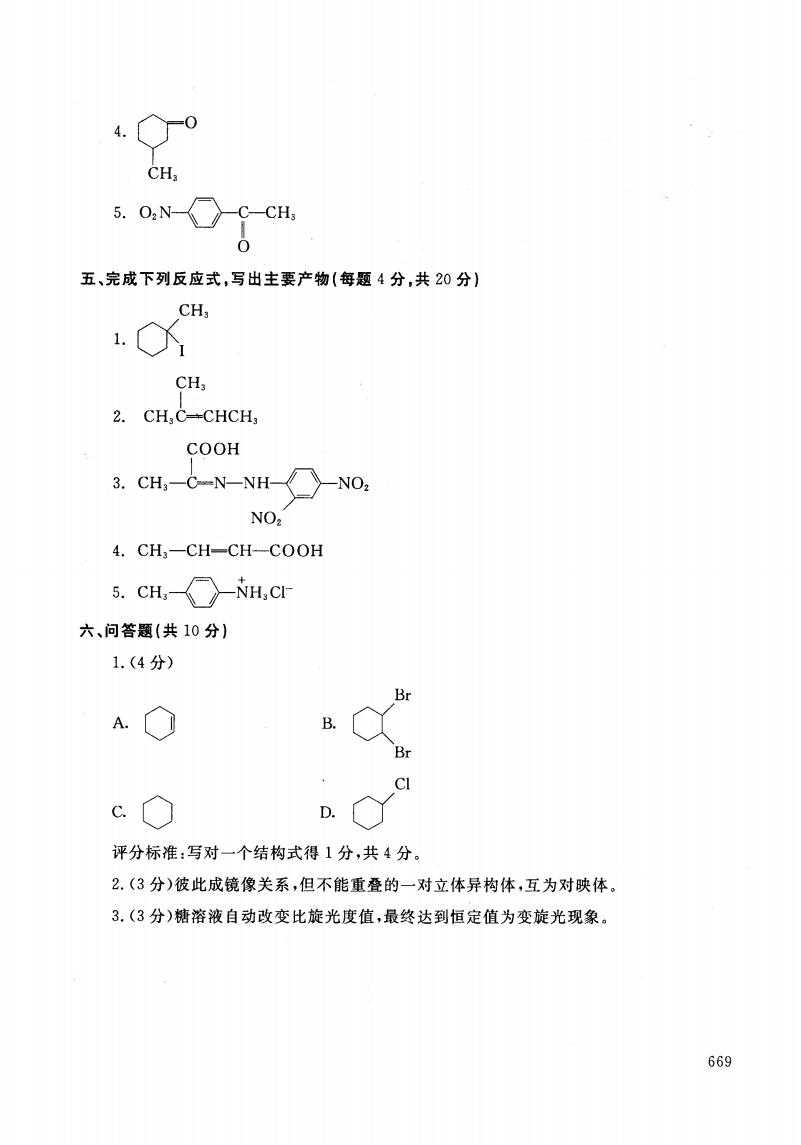
CH, 5.02N C—CH3 五、完成下列反应式,写出主要产物(每题4分,共20分)】 CH, CH, 2.CH,C-CHCH, COOH 3.CH,-6-N-NH-NO. NOz 4.CH,-CH-CH-COOH 5.CH,》-NH,C 六、问答题(共10分) 1.(4分) Br AO B. CI D. 评分标准:写对一个结构式得1分,共4分。 2.(3分)彼此成镜像关系,但不能重叠的一对立体异构体,互为对映体。 3.(3分)糖溶液自动改变比旋光度值,最终达到恒定值为变旋光现象。 669
厂尸丫} O 气 C r H.3 5. Oz N-母-C}-GH3 五、完成下列反应式 ,写出主要产物 (每题 4分,共 20分) 2. CH3C} CHCH COOH 3. CH3-C=N-N N H O-毋-NO 4. CH3- CH= CH- 000H 5. CH3-短卜 + N H Cl- 六、问答题(共 10分) 、, 产 、 1 \ 、 l se Z 孟任 1 了 L 、 A 评分标准 :写对一个结构式得 1分,共 4分 。 .(3分)彼此成镜像关系,但不能重叠的一对立体异构体,互为对映体。 . (3分)糖溶液 自动改变 比旋光度值,最终达到恒定值为变旋光现象。 669