
试卷代号:2035 座位■ 中央广播电视大学2012一2013学年度第一学期“开放专科”期末考试(开卷) 农科基础化学 试题 2013年1月 题 号 三 四 五 六 总 分 分 数 得 分 评卷人 一、单项选择题(在各题的备选答案中,只有1项是正确的,请将正确 答案的序号,填写在题中的括号内。每小题2分,共20分) 1.某一可逆反应体系采用某种催化剂以增大正反应生成物的产量,这种催化剂具有下列 哪一性质?() A.仅能增大正反应速度 B.同等程度地催化正逆反应,从而缩短达到平衡的时间 C.能使平衡常数K发生改变,从而使正反应速度加快 D.使正反应活化能较低,从而使正反应速度加快 2.误差的正确定义是()。 A.某-一测量值与其算术平均值之差 B.含有误差之值与真值之差 C.测量值与其真值之差 D.错误值与其真值之差 3.在质量分数为0.80的甲醇水溶液中,甲醇的物质的量分数接近于( A.0.3 B.-0.5 C.0.9 D.0.7 438K时,反应2A(®)=B(g,K0=3.9X103,同温度下反应A(g)=号B(g)的K应 为( )。 A.g×10 B.1.95×10-2 C.3.9×10-2 D.W3.9X10z 123
试卷代号 座位号仁口 -、单项选择题{在各题的备选答案中,只有 1项是正确的,请将正确 答案的序号,填写在题中的括号内。每小题 2分,共 0分} 中央广播电视大学 2 0 3学年度第一学期"开放专科"期末考试(开卷) 农科基础化学试题 2013 年1 |题号|一|二|三|四|五|六|总分| |分数 I I I I I I I |得分|评卷人| I I I 1.某-可逆反应体系采用某种催化剂以增大正反应生成物的产量,这种催化剂具有下列 哪一性质? ( ) A. 仅能增大正 应速 B. 度地 逆反应 平衡 C. 平衡 数K 发生改变 反应速度加 D.使正反应活化能较低,从而使正反应速度加快 2. 误差 定义 )。 A. 测量 值之差B. 真值 C. 差D. 错误值 3. 质量 为0.80 )。 A. 0.3 C. 0.9 B. 一0.5 D. 0.7 4. 384K 削ρ=Bω 0 - 下反应Aω=÷Bω )。 A. _1一X lO 3.9 C. 3. 9X 10-2 B. 1. 95 X 10-2 D. .J3.9灭百习 123

5.在吸光光度法测量中,宜选用的吸光度读数范围是()。 A.0.0~0.2 B.0.10.3 C.0.7~1.0 D.0.2≈0.7 6.下列化合物哪一个在水中溶解度最小?() A.甲酸 B.乙酸 C.丙酸 D.丁酸 7.下列化合物中能形成分子间氢键的是?() A.烷烃 B.烯烃 C.炔烃 D.醇 8.下列哪种分子是羧酸() A.CH,CH,CH,-OH B.CH,CH2-O-CH, C.CH;CH2C-OH D.CH,CH2C-CH, 0 0 9.下列化合物在浓NaOH中能发生歧化反应的是()。 A.CH CHO B.(CH,)CCOCH; C.CH,COCH, D.HCHO 10.下列化合物能与亚硫酸氢钠加成的是( )。 A.HCHO B.CH:CH2 COCH2 CH CHO D COCH, 得分 评卷人 二、判断题(每小题2分,共10分) 11.增加测定次数可减小随机误差,但不能减少系统误差。() 12.Na2SzO3不能直接滴定K2Cr2O,,滴定时首先加入过量的KI,然后用Na2S2O3标准 溶液滴定定量产生的【2。这种滴定方式叫间接滴定方式。() 13.弱酸物质的量浓度越小,离解度α越大,故pH越小。() 14.4d检验法是用来检验分析方法是否存在系统误差。() 15.已知K.(HAc)大于K.(HCN),所以CN是比Ac强的碱。() 124
5. 光光度法 宜选 读数 )。 A. o. o~o. 2 C. o. 7~ 1. 0 6. 化合 在水 最小 ( A.甲酸 C. 丙酸 7. 下列 形成 ( A. 皖腔 C. 8. 列 哪 子是援 ) B. 0.1~0. 3 D. o. 2~O. 7 B. D.丁酸 B. 烯怪 D. B. CH3CH 2-O一-CH D. CH3CH2C一CH II O 〉。 A. CH 3CH2CH2-OH C. CH3CH2C一-OH II O 9. 下列 浓NaOH 发生歧 反应 A. CH 3CHO B. (CHρ3CCOCH3 C. CH3COCH3 D. HCHO 10. 下列 能与 铀加 )。 A. HCHO B. CH 3CH2COCH 2CH3 C. ( ~CHO D. ( ) |得分|评卷人| I I I 二、判断题{每小题 2分,共 0分) 1. 增加测 次数 减小 ) 12. Na2S203 定K r2 ,滴定时首先加人过量的町,然后用 3标准 溶液滴定定量产生的 滴定 接滴 。( ) 13. 浓度 离解 越大 故pH ) 14.4d 检验法是 验分 方法是 ) 15. (HAc) 于K.(HCN) 以CN 比Ac ) 124

得分 评卷人 三、计算题(每小题10分,共30分) 16.铁矿石试样0.3073g,制成Fe2+试液后,在酸性下用c(日K,C,0,)=0.06356mol· L-1KzCr2O,标准溶液滴定,用去40.27mL,求该样中FezO3的质量分数。[已知:M(FezO3) =159.7g·mol1] 17.0.20mol·L-1 NaH2 PO,溶液10.0mL与0.25mol·L-1 Naz HPO4溶液20.0mL积 混合,求混合溶液的pH值。(已知pK,(HzPO,)=7.21) 18.计算298K时Sn+/Sn2+,c(Sn4+)=2.0mol·L1,c(Sn2+)=0.4mol·L-1电对的电 极电势。(已知p3。+s2+=0.151V) 得 分 评卷人 四、完成方程式(每小题4分,共20分) 浓HzSO4 19. +HO-NO2 50-60℃ 20. CH,CH2C-CH2 KMnO H+ CH, 21.CH,CH,COOH+NH; 22.CH:CH2CH2 OH- K:CrO:,H+ 23.CH,CH2 Cl+NH3 得分 评卷人 五、用系统命名法命名下列化合物(每个4分,共16分) C=CH 24 125
|得分|评卷人| I I I 三、计算题{每小题 0分,共 0分) 1 16. 石试样0.3073g 成Fe2+ 在 酸 下用 ( ; K2Cr20 , ) = O. 06356mol • 6 L-IK2Cr20 去40.27mL 中Fe203 质量分数 知:M( e2 03) =159. 7g • mol-I] 17. O. 20mol • L-INaH2P0 液10.0mL 与O. 25mol • L-I Na2HP0 液20.0mL 混合,求混合溶液的 H值。(已知 =7.21) 18. 算298K 4+ /Sn2+ , c( Sn4+ ) =2. Omol • L-I , c(Sn2+) =0. 4mol • L- 极电势。(已知伊t, z+ =0.151V) 得 分 I I I 四、完成方程式{每小题 4分,共 0分) 19. II I +HO-NO. lL A - 50-60 "C 20. CH3CH2C二CH CH 3 21. CH3CH2COOH+NH3 KMnO. H+ ' K2CrO"H+ 22. CH 3CH2CH20H 23. CH 3CH2Cl+ NH3 |得分|评卷人| I I I 24·6 五、用系统命名法命名下到化合物(每个 4分,共 6分) 125
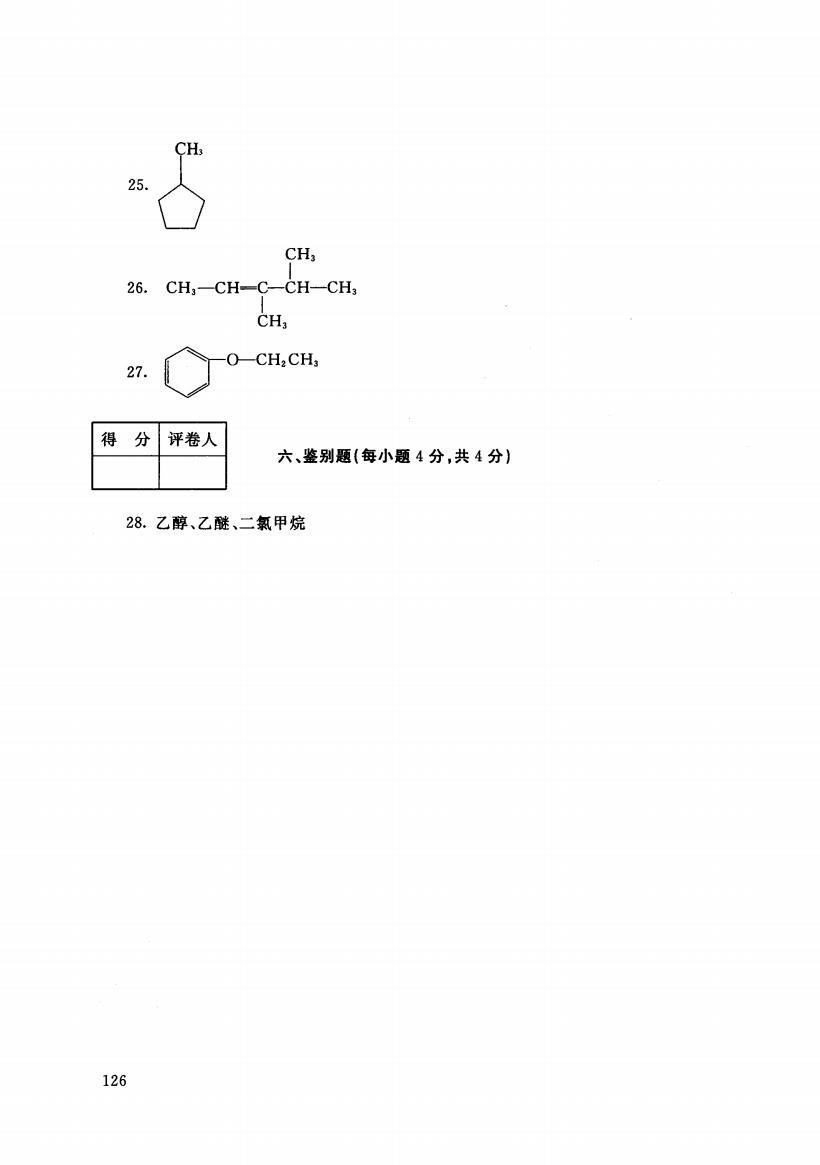
CH 25, CH, 26. CH,-CH-C-CH-CH; CH, O-CH2CH, 27. 得 分 评卷人 六、鉴别题(每小题4分,共4分) 28.乙醇、乙醚、二氯甲烷 126
253 CH3 26. CH 一CH=C CH 3 27σo- |得分|评卷人| I I I 六、鉴别题{每小题 28. 二氯 126

试卷代号:2035 中央广播电视大学2012一2013学年度第一学期“开放专科”期末考试(开卷) 农科基础化学 试题答案及评分标准 (供参考) 2013年1月 一、单项选择题(在各题的备选答案中,只有1项是正确的,请将正确答案的序号,填写在题中 的括号内。每小题2分,共20分) 1.D 2.C 3.D 4.D 5.D 6.D 7.D 8.C 9.D 10.A 二、判断题(每小题2分,共10分) 11./ 12.X 13.× 14.× 15./ 三、计算题(每小题10分,共30分) c号K,C0,)V·M2FeO,) 16.解: @(Fe2O3)=- (4分) m =0.06356X40.27X78.36×10-×100%=65.27% 0.3073 (6分) 17.解: 此混合溶液是H2PO,一HPO缓冲溶液,已知pK.(H2PO)=7.21 (2分) 混合液HzPO:和HPO?浓度分别为: cP05)288982。-0.o67nolL (2分) (Ho)-828¥88-a167mo.L (2分) pH=pk+le8号}-.21+lg68-2.21+a.40=1.61 (4分) 18.解: 已知p3+/s2+=0.151V Sn++2e=Sn2+ (2分) p=g+0.05921g(Sn 2 c(Sn2+) (4分) =0.151+0-0592g0品=0172Vy (4分) 2 127
试卷代号 3 5 中央广播电视大学 3学年度第一学期"开放专科"期末考试(开卷) 农科基础化学试题答案及评分标准 (供参考) 2013 年1 一、单项选择题{在各题的备选答案中,只有 1项是正确的,请将正确答案的序号,填写在题中 的括号内。每小题 2分,共 0分) 1.D 2. C 3.D 4.D 5.D 6.D 7.D 8. C 9.D 10. A 二、判断题{每小题 2分,共 0分} 11. .J 12. X 13. X 三、计算题{每小题 0分,共 0分} c(÷K2Crz07)·v·M(4Fez03) ω(F = V 14. X 15. .J 16. m (4 O. 06356X40. 27X78. 36X10- 3 X100%=65.27% (6 0.3073 17. 此混 是H2PO,-HPO~ 溶液 知pK.(H2PO')=7.21 (2 混合液 0.20X10 , c(H2PO, ) = n~' :v,' ~:v O. 067mol • L- 1 .~~./ 20.0 十10.0 (2 18. , O. 25X20. 0 c(HPm-) = ~~ u~' :-~. O. 167mol • L- 1 • / 20.0+10.0 c(HPO~-)O.167 pH=pK.+lg ~;;;~n~~-~ =7.21十19 ~一一一 +0.40=7.61 c(H2PO, ) .. -~ . .." O. 067 已知伊 /Snz+ =0. 151V SnH +2e=Sn2+ (2 (4 nu q" v Flw-punru- GBK (2 (4 (4 127

四、完成方程式(每小题4分,共20分) 浓HzSO, NO2+H2O 19 +HO-NOz 50-60℃ CH,CH2C-CH, KMnO 20. +CH:CH2 COCH:+CO2+H20 H+ CH, 21.CH,CH,COOH+NH, CH,CH2 CONH2 22.CH:CHCH OH K:CrO:,H →CHCH2COOH 23.CH,CH,CI+NH +CH,CH2 NH2 五、用系统命名法命名下列化合物(每个4分,共16分) 24.苯乙炔 25.甲基环戊烷 26.3,4-二甲基-2-戊烯 27.苯乙醚 六、鉴别题(每小题4分,共4分) 乙 醇 褪色 KMnO 28.乙 醚 H+ →X]浓H2S04 溶解 二氯甲烷 X 低温 不溶 128
四、完成方程式{每小题 9O 叫叩 II' ""'t- O 20. CH3CHzC二CH "CH3CHzCOCH3 +CO 十HzO CH3 21. CH 3CHzCOOH+NH3 KMnO , H+ "CH3CHzCONHz 22. CH3CHzCHzOH 23. CH 3CHzCl+NH3 KzCrO ,.H+ ----·CH3CHzCOOH "CH3CHzNH z 五、用系统命名法命名下到化合物{每个 24. 25. 戊炕 26.3 ,4- 基-2-戊烯 27. 六、鉴别题{每小题 乙醇1褪色 28. k:104 溶解 二氯甲烧) xj 128